At forstå atomnummer:definition, betydning og forskel fra atomvægt
Evgenii_Bobrov/iStock/GettyImages
I den moderne atommodel er et atom en kompakt, positivt ladet kerne, der kredser om en diffus sky af negativt ladede elektroner. Kernen huser protoner, som bærer den positive ladning, og neutroner, som er elektrisk neutrale. Antallet af protoner identificerer entydigt hvert grundstof og kaldes atomnummeret . I modsætning til atommasse eller atomvægt er atomnummeret et fast heltal for et givet grundstof og varierer ikke med isotopsammensætningen.
TL;DR
Atomnummeret er lig med protontallet i et grundstofs kerne, hvilket bestemmer dets position i det periodiske system. Atomvægt er et gennemsnit af masserne af alle naturligt forekommende isotoper og er typisk større end atomnummeret.
Det periodiske system og atomnummer
Det periodiske system arrangerer grundstoffer i stigende rækkefølge efter atomnummer. Forskere genkender i øjeblikket 118 elementer; den nyeste, oganesson (Og, atomnummer118), blev tilføjet i 2015 og produceres kun i laboratorier. Brint, med en enkelt proton, indtager den første plads. Hvert elements symbol på bordet er ledsaget af dets atomnummer, hvilket muliggør hurtig identifikation af protonantal uden at tælle positioner.
Atomnummer vs. Atommasse og Vægt
Når du konsulterer et moderne periodisk system, vil du se en anden numerisk værdi ved siden af atomnummeret. Dette er atomvægten , en gennemsnitlig masse af alle naturligt forekommende isotoper af det pågældende grundstof udtrykt i atomare masseenheder (amu). Det er forskelligt fra atommassen af en enkelt isotop, som kun summerer masserne af protoner og neutroner i kernen. Elektroner bidrager ubetydeligt til atommassen.
Fordi isotoper af et grundstof kun adskiller sig i neutrontal, har hver en unik atommasse. Atomvægten præsenteret i tabellen er et vægtet gennemsnit af disse masser, der afspejler den naturlige isotopfordeling. Mens atomnummeret er invariant, kan atomvægten således variere med ændringer i isotopsammensætningen.
Sidste artikelSikre og effektive syreneutraliseringsteknikker
Næste artikelBeregning af temperaturusikkerhed:En praktisk vejledning
 Varme artikler
Varme artikler
-
 Forskere afslører struktur og funktion af en molekylær motorKunstnerisk fremstilling af Holliday-krydset og RuvB-motorerne. Kredit:CSSB, Nicola Graf Molekylær motorer er komplekse enheder sammensat af mange forskellige dele, der forbruger energi til at udfø
Forskere afslører struktur og funktion af en molekylær motorKunstnerisk fremstilling af Holliday-krydset og RuvB-motorerne. Kredit:CSSB, Nicola Graf Molekylær motorer er komplekse enheder sammensat af mange forskellige dele, der forbruger energi til at udfø -
 Jagten på en bedre solcremeKredit:Pixabay/CC0 Public Domain Mange sommerdage starter med at smøre solcreme på for at forhindre solskoldning, hudskader og hudkræft. En almindelig ingrediens i solcremer er avobenzon, som virke
Jagten på en bedre solcremeKredit:Pixabay/CC0 Public Domain Mange sommerdage starter med at smøre solcreme på for at forhindre solskoldning, hudskader og hudkræft. En almindelig ingrediens i solcremer er avobenzon, som virke -
 Forståelse af methylendiphenylisocyanat (MDI):Produktion, anvendelser og sikkerhedMethylendiphenylisocyanat (MDI) er en vigtig isocyanatforbindelse, der hovedsageligt anvendes til fremstilling af polyurethanskum, der finder anvendelse i isolering, polstring og kompositmaterialer. D
Forståelse af methylendiphenylisocyanat (MDI):Produktion, anvendelser og sikkerhedMethylendiphenylisocyanat (MDI) er en vigtig isocyanatforbindelse, der hovedsageligt anvendes til fremstilling af polyurethanskum, der finder anvendelse i isolering, polstring og kompositmaterialer. D -
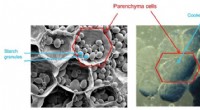 Ny forarbejdningsteknik kan gøre kartofler sundereMikroskopisk billede af kartoffelvæv før (venstre) og efter (højre) kogning eller forarbejdning. Kredit:Amy Lin, A*STAR, og Yijing Shao og YuLian Lin, University of Idaho. Forskere annoncerede tidl
Ny forarbejdningsteknik kan gøre kartofler sundereMikroskopisk billede af kartoffelvæv før (venstre) og efter (højre) kogning eller forarbejdning. Kredit:Amy Lin, A*STAR, og Yijing Shao og YuLian Lin, University of Idaho. Forskere annoncerede tidl
- Hvad bruger forskere til at opdele Suns -lyset i spektrum?
- I betragtning af at jo fjernere et objekt er mindre vinkel, vil det gøre, hvorfor ville parallax må…
- Eksempler på Nematodes
- Hvad sker der med en elektromagnetisk bølge energi, når dens frekvens øges?
- Uddybende spørgsmål:Hvad går tabt, når et sprog dør?
- Destabiliseringsprocesser i skum


