Mestring af molaritet:En trin-for-trin guide til beregning af indledende koncentrationer
Beherskelse af molaritet:En trin-for-trin guide til beregning af indledende koncentrationer
Af bidragende forfatter • Opdateret 24. marts 2022
Beregning af den indledende koncentration af en opløsning - almindeligvis kaldet molaritet - er en grundlæggende færdighed i kemi og biokemi. Molaritet udtrykker, hvor mange mol opløst stof der er til stede pr. liter opløsning.
Trin 1:Konverter massen af opløst stof til mol
Vej det opløste stof i gram, divider derefter med dets molære masse. For eksempel har natriumhydroxid (NaOH) en molær masse på 40,0 gmol⁻1. Hvis du opløser 20,0 g NaOH:
molNaOH = 20,0 g × (1mol / 40,0 g) = 0,50 mol
Trin 2:Bestem mængden af opløsningsmiddel i liter
Mål opløsningsmiddelvolumen. Hvis målingen er i milliliter, skal du konvertere til liter (1L = 1000mL). For eksempel er 500 ml opløsningsmiddel lig med:
500mL × (1L / 1000mL) = 0,500L
Trin 3:Beregn molaritet
Del mol opløst stof med opløsningsmiddelvolumenet i liter:
M = 0,50 mol / 0,500 L = 1,0 MNaOH
Opløsningen har således en molaritet på 1 M. Forøgelse af opløsningsmiddelvolumenet vil sænke molariteten, mens reduktion af den vil øge koncentrationen.
TL;DR (for lang; læste ikke)
Hold styr på enheder gennem hele beregningen – omregn gram til mol og milliliter til liter – for at undgå konverteringsfejl ved bestemmelse af molaritet.
 Varme artikler
Varme artikler
-
 Forskere bruger maskinlæring til at identificere højtydende solcellerArgonne-forskere bruger maskinlæring og datamining i forbindelse med simuleringer og eksperimenter i stor skala til at identificere nye lysabsorberende farvestofmolekyler til solcelledrevne vinduer. K
Forskere bruger maskinlæring til at identificere højtydende solcellerArgonne-forskere bruger maskinlæring og datamining i forbindelse med simuleringer og eksperimenter i stor skala til at identificere nye lysabsorberende farvestofmolekyler til solcelledrevne vinduer. K -
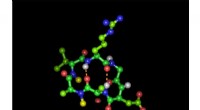 Den hellige gral af peptidkemi:Gør peptidaktive midler tilgængelige oraltCyklisk hexapeptid i sin bioaktive form med den integrinbindende tripeptidsekvens arginin-glycin-asparaginsyre:Grønne kugler repræsenterer carbonatomer, røde iltatomer, blå nitrogenatomer og hvide bri
Den hellige gral af peptidkemi:Gør peptidaktive midler tilgængelige oraltCyklisk hexapeptid i sin bioaktive form med den integrinbindende tripeptidsekvens arginin-glycin-asparaginsyre:Grønne kugler repræsenterer carbonatomer, røde iltatomer, blå nitrogenatomer og hvide bri -
 Lad det regne! Nye belægninger gør naturlige stoffer vandtætteAfvisning af forskellige væsker på polyesterstof belagt med H1F7Ma-co-DVB:sojasovs (sort dråbe), kaffe (brun dråbe), HCl -syre (øverste venstre gennemsigtige dråbe), NaOH (gennemsigtig dråbe nederst t
Lad det regne! Nye belægninger gør naturlige stoffer vandtætteAfvisning af forskellige væsker på polyesterstof belagt med H1F7Ma-co-DVB:sojasovs (sort dråbe), kaffe (brun dråbe), HCl -syre (øverste venstre gennemsigtige dråbe), NaOH (gennemsigtig dråbe nederst t -
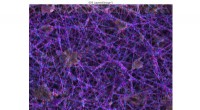 Forskningssamarbejde bringer nye koncepter for kalium-ion-batterierDette billede viser carbon nanofibre analyseret med en teknik kaldet energispredende røntgenspektroskopi efter at have gennemgået ladningsafladningscyklus i nye kaliumionbatterier. Batterierne er unde
Forskningssamarbejde bringer nye koncepter for kalium-ion-batterierDette billede viser carbon nanofibre analyseret med en teknik kaldet energispredende røntgenspektroskopi efter at have gennemgået ladningsafladningscyklus i nye kaliumionbatterier. Batterierne er unde
- Hvilken kirtel producerer kropsslim på en regnorm?
- Hvad er Columbia Plateau i Washington og Oregon?
- Parlamentsmedlemmer bør overveje online-afstemning under COVID-19-pandemien, siger forsker
- Tal forklarer, hvordan og hvorfor West bager, brænder tørrer ud
- Kan aktuelle videnskabelige metoder endeligt skelne mellem alle mikroorganismer?
- Facebook kan begynde at skjule Like -tællinger for indlæg


