Forståelse af kalorimetre:Hvordan de måler varme og deres vigtigste begrænsninger
Af John Brennan
Opdateret 24. marts 2022
Yurko_Gud/iStock/GettyImages
For kemikere er det vigtigt at kvantificere den varme, der frigives eller absorberes under en reaktion. Kalorimetre er værktøjerne, der giver den måling, hvilket muliggør en dybere indsigt i reaktionsmekanismer og mere pålidelige forudsigelser.
TL;DR
Kalorimetre kvantificerer varmen fra en reaktion. Deres største ulemper er uundgåeligt varmetab til miljøet og potentielle temperaturgradienter i prøven.
Et kalorimeters funktioner
Et kalorimeter registrerer temperaturændringen af både dens beholder og reaktanterne. Efter kalibrering giver enheden en kalorimeterkonstant, der udtrykker, hvor meget temperaturen stiger pr. tilført varmeenhed. Med denne konstant og massen af de reagerende arter kan kemikere beregne entalpiændringen af processen. Minimering af varmetab til omgivelserne er afgørende; ellers vil dataene blive skæve.
Forskellige typer kalorimetre
Mens et simpelt kaffekopkalorimeter kan bygges med to Styrofoam-kopper og et termometer, anvender akademiske laboratorier mere sofistikeret udstyr. Bombekalorimeteret placerer for eksempel reaktanterne i et forseglet stålkammer ("bomben"). En elektrisk gnist antænder blandingen, og den efterfølgende temperaturstigning afslører varmen, der udvikles eller absorberes. Hvert design er skræddersyet til specifikke reaktionstyper og krav til nøjagtighed.
Kalibrering af et kalorimeter
Kalibrering involverer at overføre en kendt mængde varme ind i systemet. En almindelig metode er blandingsvand-eksperimentet:varmt og koldt vand kombineres i kalorimeteret, og temperaturudviklingen registreres. Ved at anvende lineær regression estimeres den endelige ligevægtstemperatur. Varmen opnået af det kolde vand minus den varme tabt af det varme vand er lig med den varme, der absorberes af kalorimeteret. Ved at dividere dette tal med den samlede temperaturændring får man kalorimeterkonstanten, som derefter bruges til efterfølgende eksperimenter.
Begrænsninger af kalorimetri
Intet kalorimeter er perfekt. Selv med fremragende isolering slipper noget varme uundgåeligt ud til miljøet, hvilket medfører fejl. Ujævn blanding kan skabe temperaturgradienter, hvilket yderligere kompromitterer nøjagtigheden. Desuden er ikke alle reaktioner egnede til kalorimetrisk undersøgelse. For eksempel er den hurtige, højenergi-nedbrydning af TNT upraktisk i et simpelt kaffekopkalorimeter og kan endda udgøre sikkerhedsproblemer for et bombekalorimeter. Omvendt giver meget langsomme reaktioner, såsom oxidation af jern til rust, temperaturændringer, der er for subtile til pålidelig detektion.
 Varme artikler
Varme artikler
-
 Undervisning i det periodiske system til elever i femte klasse:En praktisk vejledningAf Lisa Magloff, opdateret 30. august 2022 I mange amerikanske skoledistrikter optræder det periodiske system først i femte klasses naturvidenskabelige læseplaner. Målet er at introducere eleverne ti
Undervisning i det periodiske system til elever i femte klasse:En praktisk vejledningAf Lisa Magloff, opdateret 30. august 2022 I mange amerikanske skoledistrikter optræder det periodiske system først i femte klasses naturvidenskabelige læseplaner. Målet er at introducere eleverne ti -
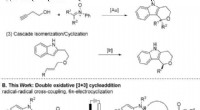 Forskere løfter sløret for en spændende ny måde at producere farmaceutiske ingredienser billiger…Tidligere udviklede syntetiske metoder og bioaktive [2, 3]‐sammensmeltede indoler. Kredit:Professor Cheol-Min Park, UNIST Et forskerhold, tilknyttet Sydkoreas Ulsan National Institute of Science a
Forskere løfter sløret for en spændende ny måde at producere farmaceutiske ingredienser billiger…Tidligere udviklede syntetiske metoder og bioaktive [2, 3]‐sammensmeltede indoler. Kredit:Professor Cheol-Min Park, UNIST Et forskerhold, tilknyttet Sydkoreas Ulsan National Institute of Science a -
 Forskere dechifrerer strukturen af lovende metalorganiske rammerForskere ved MIT og andre institutioner har fundet en måde at stabilisere væksten af krystaller af flere slags metalorganiske rammer, eller MOFer. Dette billede viser to scanning elektronmikroskopi
Forskere dechifrerer strukturen af lovende metalorganiske rammerForskere ved MIT og andre institutioner har fundet en måde at stabilisere væksten af krystaller af flere slags metalorganiske rammer, eller MOFer. Dette billede viser to scanning elektronmikroskopi -
 Hvorfor æg krymper i opløsninger med høj opløsning:En klar osmoseforklaringAf Mary Tarsi | Opdateret 24. marts 2022 Hvorfor æg krymper i opløsninger med høj opløsning Et æg vil miste volumen, når det placeres i en opløsning med en højere koncentration af opløst stof end ind
Hvorfor æg krymper i opløsninger med høj opløsning:En klar osmoseforklaringAf Mary Tarsi | Opdateret 24. marts 2022 Hvorfor æg krymper i opløsninger med høj opløsning Et æg vil miste volumen, når det placeres i en opløsning med en højere koncentration af opløst stof end ind
- En ny udsigt til briller
- Hvordan forbedrer forbedringer i mikroskopteknologier din forståelse af celleteorien?
- Nyt netto nul-emissionsmål stopper ikke Storbritanniens bidrag til global opvarmning – her er hvorf…
- Northern Taurids Meteor Shower:Hvornår, hvor og hvorfor det er værd at se
- Geovidenskabsmænd tilbyder nye beviser for, hvordan Adirondack-bjergene blev dannet
- PhenoCam -netværk udnytter store data til at forudsige indvirkningen af varmere klima på økosys…


