Hvorfor æg krymper i opløsninger med høj opløsning:En klar osmoseforklaring
Af Mary Tarsi | Opdateret 24. marts 2022
Hvorfor æg krymper i opløsninger med høj opløsning
Et æg vil miste volumen, når det placeres i en opløsning med en højere koncentration af opløst stof end inde i ægget. I en sådan opløsning bevæger opløsningsmidlet (vandet) sig ud af ægget ved osmose, hvilket får ægget til at krympe. Fænomenet demonstrerer det grundlæggende princip for cellulær vandbalance.
Trin 1:Fjern skallen
Først skal du opløse skallen med eddike. Eddikesyren reagerer med calciumcarbonatet og efterlader æggets semipermeable membran intakt.
Trin 2:Placer ægget i en opløsning
Nedsænk det skalfrie æg i en homogen blanding - f.eks. vand, majssirup eller honning. Opløsningens koncentration af opløste stoffer dikterer vandets bevægelsesretning.
Forstå osmose
Osmose er den passive strøm af vand over en semipermeabel membran fra et område med lavere koncentration af opløst stof til et område med højere koncentration, med det formål at udligne koncentrationer på begge sider. Når den eksterne opløsning er hypertonisk (højere koncentration af opløst stof), kommer vand ud af ægget, hvilket forårsager krympning. Hvis opløsningen er hypotonisk, svulmer ægget. En isotonisk opløsning holder ægget uændret.
Den semipermeable membrans rolle
Kun små molekyler som vand kan krydse membranen; større opløste molekyler (f.eks. sukker i majssirup) er udelukket. Denne selektive permeabilitet er grunden til, at ægget kan krympe i sukkerholdige opløsninger.
I undervisningsmiljøer tilbyder dette eksperiment en praktisk illustration af osmose og membranpermeabilitet.
 Varme artikler
Varme artikler
-
 Svovlsyre (H₂SO3):Formel, struktur og molekylmasse forklaretDavid Kashakhi/iStock/GettyImages Hvad er svovlsyre? Svovlsyre er en særskilt uorganisk forbindelse med formlen H₂SO₃ . I modsætning til sin mere velkendte pendant, svovlsyre (H₂SO4), er svovlsyre al
Svovlsyre (H₂SO3):Formel, struktur og molekylmasse forklaretDavid Kashakhi/iStock/GettyImages Hvad er svovlsyre? Svovlsyre er en særskilt uorganisk forbindelse med formlen H₂SO₃ . I modsætning til sin mere velkendte pendant, svovlsyre (H₂SO4), er svovlsyre al -
 Peptid-fingeraftryk muliggør tidligere diagnosticering af Alzheimers sygdomNeurale netværk kan detektere små forskelle i farvemønstrene fra tørrede peptidopløsninger (venstre:amyloid beta (Aβ42) peptid; højre:mutation). Kredit:Karlsruhe Institute of Technology Neurodegene
Peptid-fingeraftryk muliggør tidligere diagnosticering af Alzheimers sygdomNeurale netværk kan detektere små forskelle i farvemønstrene fra tørrede peptidopløsninger (venstre:amyloid beta (Aβ42) peptid; højre:mutation). Kredit:Karlsruhe Institute of Technology Neurodegene -
 Omdannelse af CO2 til brugbar energiBrookhaven-forskere er afbilledet ved NSLS-II beamline 8-ID, hvor de brugte ultrastærkt røntgenlys til at se den kemiske kompleksitet af et nyt katalytisk materiale. Fra venstre mod højre ses Klaus At
Omdannelse af CO2 til brugbar energiBrookhaven-forskere er afbilledet ved NSLS-II beamline 8-ID, hvor de brugte ultrastærkt røntgenlys til at se den kemiske kompleksitet af et nyt katalytisk materiale. Fra venstre mod højre ses Klaus At -
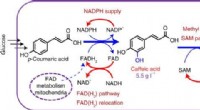 Cofactor engineering driver naturlig produktsynteseGrafisk abstrakt. Kredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01014-6 I det sidste årti har fremskridt inden for syntetisk biologi banet vejen mod bæredygtig syntese af komplekse
Cofactor engineering driver naturlig produktsynteseGrafisk abstrakt. Kredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01014-6 I det sidste årti har fremskridt inden for syntetisk biologi banet vejen mod bæredygtig syntese af komplekse


