Svovlsyre (H₂SO3):Formel, struktur og molekylmasse forklaret
David Kashakhi/iStock/GettyImages
Hvad er svovlsyre?
Svovlsyre er en særskilt uorganisk forbindelse med formlen H₂SO₃ . I modsætning til sin mere velkendte pendant, svovlsyre (H₂SO4), er svovlsyre aldrig blevet isoleret som en stabil væske; det er kun blevet påvist i gasfasen under laboratorieforhold.
Kemisk formel og molekylær struktur
En kemisk formel angiver de grundstoffer, der udgør et molekyle, og antallet af atomer af hver. For H2SO3 består strukturen af et centralt svovlatom bundet til tre oxygenatomer:to enkeltbindinger og en dobbeltbinding. De to brintatomer binder sig til de enkeltbundne oxygener, hvilket giver den samlede støkiometri af to hydrogener, et svovl og tre oxygener.
Molekylær masse
Molekylmassen (eller formelmassen) af en forbindelse er summen af de relative atommasser af dens konstituerende atomer. Ved at bruge standard atommasserne fra det periodiske system - hydrogen (1), svovl (32) og oxygen (16) - er beregningen ligetil:
Formelmasse =(2 × 1) + (1 × 32) + (3 × 16) =82
Således er svovlsyrlingens molekylvægt 82g/mol. Mens det periodiske system angiver mere præcise atommasser, der tager højde for isotopiske variationer, er afrunding til det nærmeste heltal typisk tilstrækkeligt til de fleste praktiske beregninger.
Vigtige ting
- Den korrekte formel for svovlsyrling er H₂SO₃ .
- Den har en molekylvægt på 82 g/mol.
- I modsætning til svovlsyre eksisterer svovlsyre ikke som en stabil væske; den ses kun som en gas.
 Varme artikler
Varme artikler
-
 Ny algoritme forudsiger optimale materialer blandt alle mulige forbindelserResultaterne af en Mendelevian-søgning efter hårde og superhårde materialer Kredit:Zahed Allahyari og Artem R. Oganov / NPJ Computational Materials Skoltech-forskere har tilbudt en løsning på prob
Ny algoritme forudsiger optimale materialer blandt alle mulige forbindelserResultaterne af en Mendelevian-søgning efter hårde og superhårde materialer Kredit:Zahed Allahyari og Artem R. Oganov / NPJ Computational Materials Skoltech-forskere har tilbudt en løsning på prob -
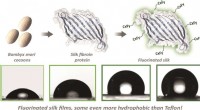 Forskere bruger modificerede silkeproteiner til at skabe nye nonstick-overfladerGrafisk abstrakt. Kredit:ChemBioChem (2022). DOI:10.1002/cbic.202200429 Forskere ved Tufts University har udviklet en metode til at lave silkebaserede materialer, der nægter at holde sig til vand,
Forskere bruger modificerede silkeproteiner til at skabe nye nonstick-overfladerGrafisk abstrakt. Kredit:ChemBioChem (2022). DOI:10.1002/cbic.202200429 Forskere ved Tufts University har udviklet en metode til at lave silkebaserede materialer, der nægter at holde sig til vand, -
 Binding af metan med metal:Et nyt håb om at genbruge det potente fossile brændstofi stand til at blive transporteret, bliver metan et biprodukt, der brændes (eller blusses) ved kilden, hvilket er både spild og uhyre forurenende. Kredit:Shutterstock UNSW kemikere har konstrueret
Binding af metan med metal:Et nyt håb om at genbruge det potente fossile brændstofi stand til at blive transporteret, bliver metan et biprodukt, der brændes (eller blusses) ved kilden, hvilket er både spild og uhyre forurenende. Kredit:Shutterstock UNSW kemikere har konstrueret -
 Ny drejeskivelignende katalytisk reaktor lover mere bæredygtig kemisk fremstillingIngeniørerne bag Spinning Mesh Disc Reactor har vundet midler til at fortsætte med at udvikle deres innovative katalytiske reaktor. Kredit:University of Bath En ny katalytisk reaktor, der hurtiger
Ny drejeskivelignende katalytisk reaktor lover mere bæredygtig kemisk fremstillingIngeniørerne bag Spinning Mesh Disc Reactor har vundet midler til at fortsætte med at udvikle deres innovative katalytiske reaktor. Kredit:University of Bath En ny katalytisk reaktor, der hurtiger
- Er det sandt eller falsk, at metallers fysiske egenskaber er uafhængige af antallet af delokalisere…
- Hvad er det bedste apparat til at veje masse?
- Hvilken kraft har et objekt i et cirkulært objekt?
- Hvilken cellulær proces kræver ikke ATP?
- Kovalente bindinger:Forståelse af elektrondeling og oktetreglen
- Hvilken forbindelse nedbrydes, når den opvarmes til zinkoxid?


