Hvorfor saltvand fremskynder metalrustning:Videnskaben bag korrosion
Af Claire Gillespie | Opdateret 24. marts 2022

Jernoxid - almindeligvis kaldet rust - er en rødbrun forbindelse, der dannes, når jern reagerer med ilt i nærvær af vand eller fugt. Når chloridioner er til stede, såsom i saltvand, sker den samme reaktion, men processen accelererer betydeligt.
TL;DR (for lang; læste ikke)
Rust er en form for korrosion drevet af elektronoverførsel. Saltvand, som er en bedre elektrolyt, fremskynder denne overførsel, så jern korroderer hurtigere end i ferskvand.
Hvordan metaller korroderer
Ikke alle metal "ruster". Aluminium udvikler for eksempel et tyndt, beskyttende oxidlag, der beskytter det mod fugt og ilt. Jern på den anden side mangler en sådan barriere, så det danner let hydreret jernoxid, når det udsættes for vand og luft.
Korrosion begynder, når jernatomer mister elektroner (oxidation), mens iltatomer får elektroner (reduktion). De resulterende jernholdige (Fe²⁺) og ferri-ioner (Fe3⁺) reagerer med vand for at producere jernhydroxider, som gradvist taber vand til dannelse af jernoxider - samlet kendt som rust. Efterhånden som rusten flager væk, afsløres frisk jern, hvilket fortsætter cyklussen.
Saltvand vs. Ferskvand
Saltvand er en overlegen elektrolyt, fordi den indeholder opløste ioner, der letter elektronstrømmen. I en elektrokemisk celle betyder det, at de anodiske (jern) og katodiske (iltreduktion) reaktioner opstår lettere. Som følge heraf korroderer jern med en hastighed op til 10-15 gange hurtigere i havvand end i ferskvand. Selv kortvarig udsættelse for saltspray eller høj luftfugtighed kan efterligne denne effekt på metalstrukturer.
Forebyggelse af korrosion i saltmiljøer
Beskyttende strategier omfatter:
- Galvanisering: Belægning af jern med zink skaber en offeranode, der fortrinsvis oxiderer og afskærmer det underliggende metal.
- Epoxy- og malingsbelægninger: Højtydende, saltbestandige malinger forsegler overfladen og blokerer for adgang til fugt og klorid.
- Katodisk beskyttelse: Installation af offeranoder eller imponerede strømsystemer tvinger metallet til at fungere som en katode, hvilket forhindrer oxidation.
- Materialevalg: Valg af iboende korrosionsbestandige legeringer såsom rustfrit stål eller aluminium kan reducere vedligeholdelsesbehovet.
Disse metoder er bredt godkendt af industristandarder såsom ASTM G1 (Standard Practice for Corrosion Testing) og NACE SP 0101 (Corrosion Prevention of Structural Steel).
Sidste artikelSvovlsyre (H₂SO3):Formel, struktur og molekylmasse forklaret
Næste artikelEffektive måder at smelte is på uden varme
 Varme artikler
Varme artikler
-
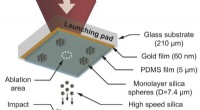 Forskere viser, at materialer styrkes af sig selv, når de påvirkes med meget høj hastighedSkematisk illustration af den laser-inducerede mikropartikel-påvirkningstest Kredit:U.S. Army Research Laboratory Forskere fra hæren og MIT avancerede en unik eksperimentel enhed for bedre at test
Forskere viser, at materialer styrkes af sig selv, når de påvirkes med meget høj hastighedSkematisk illustration af den laser-inducerede mikropartikel-påvirkningstest Kredit:U.S. Army Research Laboratory Forskere fra hæren og MIT avancerede en unik eksperimentel enhed for bedre at test -
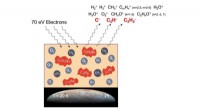 Lifes byggesten observeret i rumlignende omgivelserLavenergi-elektronpåvirkning formidler skabelsen af nye komplekse organiske molekyler, såsom ethanol, i astrofysiske/planetariske modelis indeholdende metan og ilt; mens nogle af de nye arter desorb
Lifes byggesten observeret i rumlignende omgivelserLavenergi-elektronpåvirkning formidler skabelsen af nye komplekse organiske molekyler, såsom ethanol, i astrofysiske/planetariske modelis indeholdende metan og ilt; mens nogle af de nye arter desorb -
 Krystallisering blev krystalklarKorrelation mellem cryo-transmission elektronmikroskop (TEM) billeder og krystalstrukturen. a) TEM -billede, der viser tre kolliderende klynger. Skalaen er 10 nm. b) Relative positioner af molekyler a
Krystallisering blev krystalklarKorrelation mellem cryo-transmission elektronmikroskop (TEM) billeder og krystalstrukturen. a) TEM -billede, der viser tre kolliderende klynger. Skalaen er 10 nm. b) Relative positioner af molekyler a -
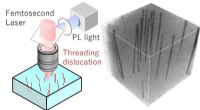 Ikke -destruktiv karakteriseringsteknik hjælper udviklingen af galliumnitridkrystalFig. 1. Målesystem og observationsbillede af TDer i GaN -halvleder ved fotoluminescensmetode med multiphoton -excitation. TDer observeres som mørke linjer. Kredit:Osaka University Fig. 1. Målesystem o
Ikke -destruktiv karakteriseringsteknik hjælper udviklingen af galliumnitridkrystalFig. 1. Målesystem og observationsbillede af TDer i GaN -halvleder ved fotoluminescensmetode med multiphoton -excitation. TDer observeres som mørke linjer. Kredit:Osaka University Fig. 1. Målesystem o
- Hvad er de 4 hovedkategorier af makromolekyler i en celle?
- Afgrøder i Frankrig viste sig at trives på trods af reduceret brug af pesticider
- Hvad er 79 kg i sten og pund?
- Hvad får magma i en subduktionszone til at stige?
- Undersøgelse bruger ændringer i Hudson River kan give indsigt i, hvordan gletsjere voksede
- Sådan beregnes center of mass


