Sådan bestemmes frysepunktet for enhver væske
Af Kevin Beck | Opdateret 24. marts 2022
Besjunior/iStock/GettyImages
Alle har været vidne til forvandlingen af en væske til fast is eller omvendt. At forstå, hvornår denne faseændring indtræffer, er afgørende for hverdagen, fra sikker kørsel om vinteren til madlavning og videnskabelige eksperimenter.
Hvad fryser og smelter?
De fleste stoffer findes i tre faser - fast, flydende eller gas - afhængigt af temperatur og tryk. Vand er unikt ved, at det kan være fast og flydende ved behageligt lave temperaturer, og det bliver til gas ved 100°C (212°F), en temperatur, der er tilgængelig for de fleste mennesker. Overgangen fra fast til flydende kaldes smeltning; det modsatte, fra flydende til fast, er frysning eller størkning. Når en væske bliver til en gas, er den koger , mens den omvendte proces er kondensering . I sjældne tilfælde kan et fast stof omgå den flydende fase og blive direkte til gas gennem sublimering , eller en gas kan aflejres direkte på en fast overflade.
Hvad påvirker fryse- og smeltepunkter?
Et stofs frysepunkt afhænger af dets molekylære struktur. For eksempel har vand et relativt højt frysepunkt på 0°C, fordi dets hydrogenbindinger let "låses" sammen, hvorimod ethylalkohol (CH₃CH₂OH) fryser ved -114°C (–174°F). Når forskellige væsker blandes, eller når et fast stof opløses i en væske, ændres den resulterende blandings frysepunkt forudsigeligt baseret på de involverede komponenter.
Opløste stoffer, opløsningsmidler og opløsninger
I en opløsning kaldes det opløste faste stof for opløst stof og væsken, der bærer det, er opløsningsmidlet . Tilsætning af et opløst stof sænker opløsningsmidlets frysepunkt – et fænomen kendt som frysepunktsdepression , en klassisk koligativ egenskab . Effekten afhænger af antallet af partikler produceret af det opløste stof, ikke af dets kemiske identitet.
Frysepunkt for NaCl-opløsning
Bordsalt (natriumchlorid) opløses i vand og reducerer dets frysepunkt, hvorfor vejfolk spreder salt om vinteren for at smelte is. NaCl dissocieres i to ioner (Na⁺ og Cl⁻), så hvert mol salt giver to partikler, der sænker frysepunktet. Et opløst stof, der producerer flere partikler pr. formelenhed, ville sænke frysepunktet endnu mere.
Frysepunktberegner
Brug en online frysepunktberegner til at slå op på temperaturerne for almindelige væsker i Celsius, Fahrenheit og Kelvin. Sammenligning af frysepunkterne for forskellige stoffer kan afsløre mønstre forbundet med deres molekylære strukturer.
 Varme artikler
Varme artikler
-
 Overgangsmetaller vs. indre overgangsmetaller:Nøgleforskelle forklaretAf Angie Chipera Opdateret 24. marts 2022 Mens både overgangsmetaller og indre overgangsmetaller optager tilstødende blokke i det periodiske system, divergerer deres elektroniske konfigurationer og r
Overgangsmetaller vs. indre overgangsmetaller:Nøgleforskelle forklaretAf Angie Chipera Opdateret 24. marts 2022 Mens både overgangsmetaller og indre overgangsmetaller optager tilstødende blokke i det periodiske system, divergerer deres elektroniske konfigurationer og r -
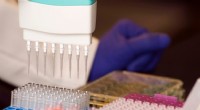
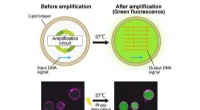 Ny kapacitet til DNA -forstærkning giver løfte om bekæmpelse af sygdommeDNA -amplifikationsproces i kunstige celler. Kredit:Yusuke Sato, Tokyo Institute of Technology DNA -amplifikation - en molekylær fotokopiering teknik, hvor genetisk materiale replikeres - har mang
Ny kapacitet til DNA -forstærkning giver løfte om bekæmpelse af sygdommeDNA -amplifikationsproces i kunstige celler. Kredit:Yusuke Sato, Tokyo Institute of Technology DNA -amplifikation - en molekylær fotokopiering teknik, hvor genetisk materiale replikeres - har mang -
 En mulig afslutning på evige kemikalierKredit:Marla Bereni/UCR Syntetiske kemikalier kendt som per- og polyfluoralkyler, eller PFAS, indeholder bindinger mellem kulstof- og fluoratomer, der anses for at være de stærkeste i organisk kem
En mulig afslutning på evige kemikalierKredit:Marla Bereni/UCR Syntetiske kemikalier kendt som per- og polyfluoralkyler, eller PFAS, indeholder bindinger mellem kulstof- og fluoratomer, der anses for at være de stærkeste i organisk kem -
 Forskere bygger robotforsker, der allerede har opdaget en ny katalysatorMobil robotforsker læsser et stativ med eksperimentelle prøver. Kredit:University of Liverpool Forskere ved University of Liverpool har bygget en intelligent mobil robotforsker, der kan arbejde 24
Forskere bygger robotforsker, der allerede har opdaget en ny katalysatorMobil robotforsker læsser et stativ med eksperimentelle prøver. Kredit:University of Liverpool Forskere ved University of Liverpool har bygget en intelligent mobil robotforsker, der kan arbejde 24
- Ræver fordampning af en væske tempelse?
- Hvad betyder det, hvis plantecellerne turgid?
- Forsyningsselskaber begynder at investere i store batterier i stedet for at bygge nye kraftværker
- Hvilke sikkerhedssymboler ville forvente at se for et eksperiment, der kræver anvendelse af syre?
- Observationer viser, at marine skyer forstærker opvarmningen
- Hvad er et Quartz Watch?


