Hvorfor isens temperatur forbliver 32°F, mens den smelter
Af Chris Deziel , Opdateret 24. marts 2022
sumos/iStock/GettyImages
Hvis den omgivende temperatur omkring et stykke is stiger, stiger isens temperatur tilsvarende. Denne stigning standser dog i det øjeblik, isen når sit smeltepunkt - 32°F (0°C). I det øjeblik gennemgår isen en faseovergang, der omdannes til flydende vand, mens dens temperatur forbliver fast, indtil det hele er smeltet. Et simpelt eksperiment viser dette:Lad en kop isterninger stå i en varm bil og overvåg temperaturen med et termometer. Det iskolde vand forbliver ved 32°F, indtil det er helt smeltet; derefter stiger temperaturen hurtigt, da den resterende væske fortsætter med at absorbere varme fra bilens interiør.
TL;DR (for lang; læste ikke)
Når du opvarmer is, stiger dens temperatur, indtil den når 32°F, og forbliver derefter konstant, mens den smelter. Den tilføjede varme bryder krystalgitterbindingerne i stedet for at øge den kinetiske energi.
Faseændringer forbruger energi
Opvarmning af is øger dens molekylers kinetiske energi, hvilket får dem til at vibrere hurtigere. Indtil smeltepunktet er nået, forstærker denne ekstra energi blot vibration; molekylerne kan endnu ikke bryde de gitterbindinger, der holder dem i en fast struktur. Når isen når 32°F, får molekylerne nok energi til at løsne sig fra gitteret. Al den tilførte varmeenergi forbruges derfor af faseovergangen, ikke ved at hæve væskens kinetiske energi. Vandets temperatur forbliver derfor på 32°F, indtil hver krystal er smeltet.
Det samme princip gælder for kogende vand. Det vil varme op til 212°F (100°C), men vil ikke overstige denne temperatur, før hver dråbe er blevet til damp. Så længe der er flydende vand i gryden, forbliver dens temperatur på 212°F uanset varmekildens intensitet.
Ligevægt ved smeltepunktet
Du kan antage, at en blanding af is og vand ville varme ensartet op, men i virkeligheden forbliver temperaturen i nærheden af isen låst ved smeltepunktet. I en stor beholder med vand med en isterning kan størstedelen af vandet stige til over 32°F, men isens umiddelbare omgivelser forbliver på den konstante temperatur. Denne ligevægt opstår, fordi når isen smelter, fryser noget af det omgivende vand igen, hvilket afbalancerer varmestrømmen. Nettoresultatet er, at den samlede temperatur ikke stiger, før al is er forsvundet.
Ud over smeltning:Tilføjelse af varme og tryk
Indføring af mere varme kan stadig producere en lineær temperaturstigning; isen vil smelte hurtigere, og temperaturen på den resterende væske vil stige. Imidlertid dominerer den varme, der kræves for at bryde gitterbindingerne, indtil faseændringen er fuldstændig.
Presset spiller også en afgørende rolle. Ved at indeslutte damp i en forseglet beholder hæver du kogepunktet, så vandet forbliver flydende ved temperaturer over 212°F. Dette er princippet bag trykkogere og industrielle dampkedler.
 Varme artikler
Varme artikler
-
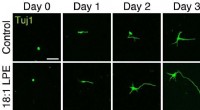 Oleoyl-LPE udøver neuritstimulering og neurobeskyttelseNeuritforlængelse, der fremmer handling Kredit:2021, Hisano et al., Shinshu universitet Lysophospholipider er fosfolipider, der kun har én fedtsyrekæde, og i de senere år, lysophospholipiders roll
Oleoyl-LPE udøver neuritstimulering og neurobeskyttelseNeuritforlængelse, der fremmer handling Kredit:2021, Hisano et al., Shinshu universitet Lysophospholipider er fosfolipider, der kun har én fedtsyrekæde, og i de senere år, lysophospholipiders roll -
 Proteinkæder, der selv dannes til spiralformede fletningerSEM-mikrofotografier af fletningstopologier observeret i geler af 2. a, Tegneseriediagrammer, der viser tostrengede sammenfiltringer og deres tilsvarende flettede ord. Fletningsordet beskriver mønster
Proteinkæder, der selv dannes til spiralformede fletningerSEM-mikrofotografier af fletningstopologier observeret i geler af 2. a, Tegneseriediagrammer, der viser tostrengede sammenfiltringer og deres tilsvarende flettede ord. Fletningsordet beskriver mønster -
 Chiralitet i realtidEn illustration af chiralitet i et molekyle. Kredit:M. Oppermann, EPFL At skelne mellem venstrehåndede og højrehåndede (chirale) molekyler er afgørende i kemi og biovidenskab, og opnås almindeligv
Chiralitet i realtidEn illustration af chiralitet i et molekyle. Kredit:M. Oppermann, EPFL At skelne mellem venstrehåndede og højrehåndede (chirale) molekyler er afgørende i kemi og biovidenskab, og opnås almindeligv -
 Genovervejelse af skadeproduktion og strålingsblanding i materialerTil venstre:Illustration af antallet af defekter i materialer forudsagt af den gamle Kinchin-Pease-ligning; Til højre:Illustration af det faktiske antal resterende skader, i overensstemmelse med forud
Genovervejelse af skadeproduktion og strålingsblanding i materialerTil venstre:Illustration af antallet af defekter i materialer forudsagt af den gamle Kinchin-Pease-ligning; Til højre:Illustration af det faktiske antal resterende skader, i overensstemmelse med forud
- Hall -effekten forbinder superledning og kvantekritikalitet i et mærkeligt metal
- Hvad bliver lysets hastighed i glas?
- Er en zygote haploid celle eller diploid?
- Hvad er formeltemperaturen?
- Forskere finder, at grønlandske gletsjersmeltevand er rigt på kviksølv
- Rødvin resveratrol kunne hjælpe Mars opdagelsesrejsende forblive stærke


