Trin-for-trin guide til fremstilling af en 0,5N saltsyreopløsning
Af Kylene Arnold – Opdateret 24. marts 2022
Normalitet udtrykker antallet af ækvivalente hydrogenioner frigivet af en liter af en syre i nærvær af en base. For stærke syrer, såsom saltsyre (HCl), er denne metrik at foretrække frem for molaritet, fordi den står for den enkelte proton, hvert molekyle donerer. En 0,5N HCl-opløsning indeholder derfor en halv ækvivalent hydrogenioner pr. liter, hvilket sikrer ensartet reaktivitet på tværs af præparater.
Trin 1 – Beregn molmassen af HCl
Sum atommasserne:brint (1,007 gmol⁻¹) + chlor (35,45 gmol⁻¹) =36,457 gmol⁻¹.
Trin 2 – Bestem den ækvivalente masse
Fordi hvert HCl-molekyle frigiver et H⁺, er den ækvivalente masse lig med den molære masse:36,457geq⁻¹.
Trin 3 – Beregn den nødvendige masse af ren HCl
Brug formlen:× (EqM × N × L). For 1L 0,5N opløsning, 36,457geq⁻¹ × 0,5N × 1L =18,2285g ren HCl.
Trin 4 – Juster for kommerciel koncentration
Kommerciel HCl er typisk 37% vægt/vægt med en specifik vægtfylde på 1,19 gmL⁻1. Beregn mængden af krævet stamsyre:18,2285g ÷ (0,37 × 1,19) =41,4mL.
Trin 5 – Forbered den fungerende løsning
1. Fyld et bægerglas med destilleret vand til ca. 500 ml (halvdelen af målvolumenet). 2. Tilsæt de 41,4 ml koncentreret HCl langsomt under konstant omrøring for at undgå lokal overophedning. 3. Når den er fuldstændig blandet, toppes opløsningen med destilleret vand for at nå præcis 1L.
Ting påkrævet
- Periodisk tabel over elementer (til reference)
- Bægerglas eller målekolbe
- Destilleret vand
- Rørestang eller magnetomrører
- Beskyttelseshandsker, beskyttelsesbriller og laboratoriefrakke (sikkerhed først)
Følg alle laboratoriesikkerhedsprotokoller ved håndtering af koncentrerede syrer, og bortskaf overskydende opløsning i overensstemmelse med lokale regler.
Sidste artikelHDPE vs. polyethylen:nøgleforskelle og anvendelser
Næste artikelByg din egen akvarie sump:En trin-for-trin guide
 Varme artikler
Varme artikler
-
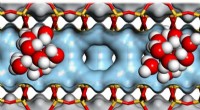 Katalyserer omdannelsen af biomasse til biobrændstofKlynger af vandmolekyler i zeoliternes hulrum hjælper med at katalysere omdannelsen af biomasse til biobrændstof. Kredit:Andreas Jentys / TUM Zeolitter er ekstremt porøse materialer:Ti gram kan
Katalyserer omdannelsen af biomasse til biobrændstofKlynger af vandmolekyler i zeoliternes hulrum hjælper med at katalysere omdannelsen af biomasse til biobrændstof. Kredit:Andreas Jentys / TUM Zeolitter er ekstremt porøse materialer:Ti gram kan -
 Forskerhold dechifrerer enzymatisk nedbrydning af sukker fra marine algerEnzymer er biokatalysatorer, der er afgørende for nedbrydningen af tangbiomasse i havene. For første gang, et internationalt hold af 19 forskere afkodede for nylig den komplette nedbrydningsvej for
Forskerhold dechifrerer enzymatisk nedbrydning af sukker fra marine algerEnzymer er biokatalysatorer, der er afgørende for nedbrydningen af tangbiomasse i havene. For første gang, et internationalt hold af 19 forskere afkodede for nylig den komplette nedbrydningsvej for -
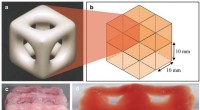 3-D-print skaber superbløde strukturer, der kopierer hjerne og lungerStruktur af en enkelt enhed; hvordan otte enheder passer sammen; to visninger af en trykt og fast struktur med otte enheder. Kredit:Imperial College London En ny 3D-printteknik gør det muligt for
3-D-print skaber superbløde strukturer, der kopierer hjerne og lungerStruktur af en enkelt enhed; hvordan otte enheder passer sammen; to visninger af en trykt og fast struktur med otte enheder. Kredit:Imperial College London En ny 3D-printteknik gør det muligt for -
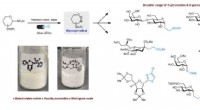 Aktivering af synligt lys muliggør transformation af bordstabile sulfoner til værdifulde glykoside…Skematisk, der viser designet af et synligt lys-medieret system til at krydskoble forskellige elektrofiler med glycosylradikaler afledt af bench-stabile heteroarylsulfoner. Kredit:Nature Synthesis (20
Aktivering af synligt lys muliggør transformation af bordstabile sulfoner til værdifulde glykoside…Skematisk, der viser designet af et synligt lys-medieret system til at krydskoble forskellige elektrofiler med glycosylradikaler afledt af bench-stabile heteroarylsulfoner. Kredit:Nature Synthesis (20
- NASA ser vindskydning stadig ramme den tropiske storm Iselle
- Hvis et objekt, der rejser i en retning, har en positiv hastighed, hvilken slags ville det samme mod…
- Hvilken formel, der bruges til at beregne, hvor meget et objekt vejer?
- Dannelse af natrium-klorbinding:Elektronoverførsel forklaret
- Klæbende situation:Ny proces forvandler trærester til tape
- Hvordan er DNA relateret til kromosomerne i kerne i en celle?


