Hvordan majssirup forbedrer bobledannelse:Videnskaben bag stærkere, længerevarende bobler
Af Geoff Hineman • Opdateret 24. marts 2022
Mens vand er rygraden i enhver bobleopløsning, omdanner tilsætningen af majssirup en simpel blanding til en formel, der er i stand til at producere større, længerevarende bobler. Nøglen ligger ikke i dets ingredienser i sig selv, men i dets fysiske egenskaber og hvordan de interagerer med vand og sæbe.
Vands polaritet og dets rolle i bobledannelse
Vandmolekyler er polære, hvilket betyder, at hvert molekyle bærer en lille positiv og negativ ladning. Denne polaritet skaber stærke brintbindinger, der får vandmolekyler til at klæbe til hinanden - et fænomen kendt som kohæsion. Sammenhængskræfterne giver vandet en udtalt overfladespænding, som er det usynlige elastiske lag, der modstår at blive strakt.
Overfladespænding:The Barrier to Bubbles
På grund af overfladespænding danner en dråbe vand en næsten perfekt kugle; kraften holder overfladen tæt bundet. Denne modstand forklarer, hvorfor en flue kan gå på vandet - overfladespændingen er stærkere end fluens vægt. Rent vand kan dog ikke uden videre danne bobler, fordi dets overfladespænding er for høj.
Sæbe:Weakening the Bonds
Når sæbe tilsættes, indsætter den sig selv mellem vandmolekyler. Sæbemolekyler har et hydrofilt (vandelskende) hoved og en hydrofob (vandafvisende) hale. Halerne trækker vandmolekyler fra hinanden, hvilket dramatisk reducerer overfladespændingen. Resultatet er en tynd film, der kan strække sig rundt om luft og skabe en boble.
Majssirup:Tilføjelse af tykkelse og stabilitet
Introduktion af majssirup - en uigennemsigtig, stivelsesholdig væske - i sæbe-vand-blandingen ændrer dynamikken yderligere. Dens høje viskositet fortykker opløsningen, så sæbefilmen bliver mere elastisk og kan holde til større bobler. Siruppens sukkermolekyler forstyrrer også den hurtige fordampning af det tynde vandlag fanget inde i en boble, hvilket giver bobler en længere levetid.
Fordampningseffekten
Alle bobler brister til sidst, fordi vandet inde i filmen fordamper. Med majssirup til stede forløber fordampningen langsommere, hvorfor bobler ser ud til at holde deres form længere. Når vandet er forsvundet, falder filmen sammen, og boblen springer.
 Varme artikler
Varme artikler
-
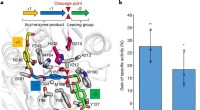 Konstrueret enzym i stand til at nedbryde PET på ti timeren, Strukturel model af 2-HE (MHET) 3 (farvet pindmodel) forankret i vildtype LCC (gråt bånd). Det formodede substratbindingssted for LCC kan opdeles i tre undersider (-2, −1, +1), hver i kontakt med
Konstrueret enzym i stand til at nedbryde PET på ti timeren, Strukturel model af 2-HE (MHET) 3 (farvet pindmodel) forankret i vildtype LCC (gråt bånd). Det formodede substratbindingssted for LCC kan opdeles i tre undersider (-2, −1, +1), hver i kontakt med -
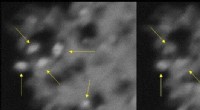 Usædvanlige nanopartikler kan gavne søgen efter at bygge en kvantecomputerPilene peger på, at titandioxid nanokrystaller lyser og blinker (venstre) og derefter falmer (højre). Kredit:Tewodros Asefa og Eliska Mikmekova Forestil dig små krystaller, der blinker som ildflue
Usædvanlige nanopartikler kan gavne søgen efter at bygge en kvantecomputerPilene peger på, at titandioxid nanokrystaller lyser og blinker (venstre) og derefter falmer (højre). Kredit:Tewodros Asefa og Eliska Mikmekova Forestil dig små krystaller, der blinker som ildflue -
 Fund tilbyder opskrift på finjustering af legeringer til brug ved høj temperaturEt stykke legering er stresstestet i Levente Vitos laboratorium ved KTH Royal Institute of Technology. Kredit:Levente Vitos Superlegeringer, der tåler ekstremt høje temperaturer, kunne snart blive
Fund tilbyder opskrift på finjustering af legeringer til brug ved høj temperaturEt stykke legering er stresstestet i Levente Vitos laboratorium ved KTH Royal Institute of Technology. Kredit:Levente Vitos Superlegeringer, der tåler ekstremt høje temperaturer, kunne snart blive -
 Kemikere producerer nye oxidanter som et værktøj til præparativ kemiKredit: Angewandte Chemie (2020). DOI:10.1002/ange.202002768 Kemisk oxidation, selektiv fjernelse af elektroner fra et substrat, repræsenterer en af de vigtigste transformationer i kemi. Imidle
Kemikere producerer nye oxidanter som et værktøj til præparativ kemiKredit: Angewandte Chemie (2020). DOI:10.1002/ange.202002768 Kemisk oxidation, selektiv fjernelse af elektroner fra et substrat, repræsenterer en af de vigtigste transformationer i kemi. Imidle
- Hvilket mikroskop bruger en stråle elektroner i stedet lys?
- Sådan beregnes mængden af et pulver Mixture
- Ny teknik til at udforske strukturelle dynamikker i nanoworld
- Hvad er de tidlige mennesker, hvis ideer om stjerner måne og sol?
- Nøjagtig måling af pH i citronsaft:en trin-for-trin guide
- Bringer de fleste protein- og aminosyrerhormoner deres virkning ved at interagere med vores gener.?


