Sådan beregnes relativ masse af atomer og molekyler
Sådan beregnes relativ masse af atomer og molekyler
Relativ masse er en hjørnesten i moderne kemi, der gør det muligt for kemikere at udtrykke massen af et atom eller molekyle i forhold til en universel standard:en-tolvtedel af et kulstof-12-atom. Fordi protoner og neutroner er omtrent 1×10⁻²⁷kg og elektroner er 1×10⁻³⁰kg, gør beregningerne både intuitive og præcise ved brug af en simpel skala uden enhed.
Hvad er relativ masse?
I dette system tæller hver proton eller neutron som 1 enhed. Elektroner, der er langt lettere, udelades fra beregningen. Således er den relative atommasse af et grundstof simpelthen summen af dets protoner og neutroner:
Relativ atommasse =antal protoner + antal neutroner
For eksempel har et brintatom (1 proton, 0 neutroner) en relativ masse på 1, mens et carbon-12-atom (6 protoner, 6 neutroner) har en relativ masse på 12.
Bestemmelse af den relative masse af et grundstof
Periodiske tabel viser en enkelt værdi for hvert element, ofte et ikke-heltal, fordi de fleste grundstoffer eksisterer som en blanding af isotoper. Tabelværdien er et vægtet gennemsnit baseret på naturlig overflod:
Vægtet gennemsnit =Σ (isotopmasse × abundance) / 100
For klor er beregningen:
((35×75) + (37×25)) / 100 =35,5
Den relative atommasse vist for chlor er således 35,5.
Relativ atommasse af specifikke isotoper
Når der refereres til en bestemt isotop – såsom uran-238 -tallet efter elementnavnet er dets nøjagtige relative masse (238). Når du kender isotopen, kan du beregne massen direkte ved at tilføje protoner og neutroner.
Beregning af relativ molekylær masse
Når de relative atommasser er kendt, er den relative molekylmasse af en forbindelse summen af hvert elements bidrag:
Relativ molekylmasse =Σ (antal atomer af grundstof × relativ atommasse af dette grundstof)
Eksempler:
- Vand (H₂O) → (2×1) + (1×16) =18
- Svovlsyre (H₂SO₄) → (2×1) + (1×32) + (4×16) =98
Anvend den samme procedure til enhver kemisk formel.
Praktiske tips
- Brug det nederste tal i det periodiske system til hurtig reference, medmindre en specifik isotop er påkrævet.
- Husk, at værdierne er enhedsløse; de repræsenterer multipla af kulstof-12-standarden.
- For komplekse molekyler kan opdeling af formlen i grupper (f.eks. CH₂, OH) forenkle beregninger.
Med disse principper kan du trygt bestemme den relative masse af ethvert atom eller molekyle, uanset om det er i akademisk forskning eller daglige kemiopgaver.
 Varme artikler
Varme artikler
-
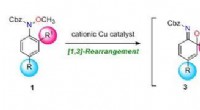 Effektiv syntese af multisubstituerede aniliner ved domino-omlejringMultisubstituerede aniliner (ortho-anisidiner). Kredit:Tohoku University Aniliner er blevet meget brugt i medicin, især i acetaminophen smertestillende midler. De bruges også i organiske materiale
Effektiv syntese af multisubstituerede aniliner ved domino-omlejringMultisubstituerede aniliner (ortho-anisidiner). Kredit:Tohoku University Aniliner er blevet meget brugt i medicin, især i acetaminophen smertestillende midler. De bruges også i organiske materiale -
 Et nyt værktøj til styring af reaktioner i mikrorobotter og mikroreaktorerThomas Russell og Ganhua Xie ved UMass Amherst og Lawrence Berkeley National Lab bruger kapillære kræfter til at udvikle en simpel metode til fremstilling af selvsamlende hængende dråber af en vandig
Et nyt værktøj til styring af reaktioner i mikrorobotter og mikroreaktorerThomas Russell og Ganhua Xie ved UMass Amherst og Lawrence Berkeley National Lab bruger kapillære kræfter til at udvikle en simpel metode til fremstilling af selvsamlende hængende dråber af en vandig -
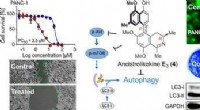 Rainforest vinforbindelse udsulter bugspytkirtelkræftcellerKredit:American Chemical Society Bugspytkirtelkræftceller er kendt for deres evne til at trives under ekstreme forhold med lave næringsstoffer og ilt, en egenskab kendt på kræftområdet som nøjsomh
Rainforest vinforbindelse udsulter bugspytkirtelkræftcellerKredit:American Chemical Society Bugspytkirtelkræftceller er kendt for deres evne til at trives under ekstreme forhold med lave næringsstoffer og ilt, en egenskab kendt på kræftområdet som nøjsomh -
 Sammensætning af multikomponentlegeringer ved screening med høj gennemstrømningFigur 1:(a) Skematisk diagram over høj gennemløb, (b) fysisk skygge maske. Kredit:© Science China Press Multikomponentmaterialer er blandt de mest lovende materialer inden for teknik og biomedicin
Sammensætning af multikomponentlegeringer ved screening med høj gennemstrømningFigur 1:(a) Skematisk diagram over høj gennemløb, (b) fysisk skygge maske. Kredit:© Science China Press Multikomponentmaterialer er blandt de mest lovende materialer inden for teknik og biomedicin
- Sådan bruger du et Fluke-multimeter:En professionel vejledning
- Det mægtige Banyan -træ kan gå og leve i århundreder
- Ny forskning viser, at grafen kan fungere som overfladeaktivt stof
- Molekyler bevæger sig hurtigere på et ujævnt terræn
- Undersøgelse undersøger, hvordan opfattet nærhed af klimaændringer påvirker meninger
- Hvor længe har Apollo 13 været i rummet?


