Sådan beregnes procentdelen af ionisering af svage syrer og baser
Af Donny Quinn, Opdateret 24. marts 2022
Billedkredit:kirisa99/iStock/GettyImages
Stærke syrer og baser dissocieres fuldstændigt i vandig opløsning, hvilket betyder, at hvert surt molekyle donerer en proton, eller hvert alkalisk molekyle frigiver en hydroxidion. Svage syrer, såsom flussyre, og svage baser, såsom ammoniak, dissocierer kun delvist. Beregning af procentdelen af dissociation – andelen af molekyler, der ioniserer – giver indsigt i deres adfærd.
Trin 1:Bestem mængden af dissocierede arter
I mange problemer leveres denne værdi direkte. I mere avancerede sammenhænge skal du muligvis udlede det fra ligevægtsudtryk eller eksperimentelle data.
Trin 2:Divider med den oprindelige koncentration
Tag mol-per-liter af dissocierede arter og divider med de oprindelige mol-per-liter af syren eller basen. Startkoncentrationen er normalt angivet på reagensetiketten eller i problemformuleringen.
Trin 3:Konverter til en procentdel
Gang resultatet med 100 for at udtrykke ioniseringsgraden i procent.
TL;DR
Når den direkte dissociationsværdi ikke er givet, bliver du nødt til at arbejde gennem ligevægtsudtryk - ofte ved at bruge syredissociationskonstanten (Ka )—for at beregne den procentvise dissociation.
At forstå denne beregning hjælper kemikere med at forudsige, hvordan svage syrer og baser opfører sig i opløsning.
 Varme artikler
Varme artikler
-
 Forskere udvikler en ny tilgang til at forudsige, hvordan væsker fryserKredit:Pixabay/CC0 Public Domain Forskere fra Queen Mary University of London har udviklet en ny beregningsmetode til bedre at forstå frysning i forskellige typer væsker. Processen med at fryse,
Forskere udvikler en ny tilgang til at forudsige, hvordan væsker fryserKredit:Pixabay/CC0 Public Domain Forskere fra Queen Mary University of London har udviklet en ny beregningsmetode til bedre at forstå frysning i forskellige typer væsker. Processen med at fryse, -
 Maskinlæring muliggør et hidtil uset kig på polymerer, der er nyttige inden for biomedicinsk områ…Et team af forskere har udviklet en metode til at undersøge strukturerne af polymerer, der er følsomme over for ydre stimuli. Venstre til højre, Yaxin An, Karteek Bejagam, og Sanket Deshmukh. Kredit:V
Maskinlæring muliggør et hidtil uset kig på polymerer, der er nyttige inden for biomedicinsk områ…Et team af forskere har udviklet en metode til at undersøge strukturerne af polymerer, der er følsomme over for ydre stimuli. Venstre til højre, Yaxin An, Karteek Bejagam, og Sanket Deshmukh. Kredit:V -
 Trin-for-trin guide til fremstilling af celluloseacetatAf Kevin Beck Opdateret 24. marts 2022 Besiki Kavtaradze/iStock/GettyImages Celluloseacetat er et stof, der ligesom en række andre materialer, der anvendes i den menneskelige industri, skylder sin
Trin-for-trin guide til fremstilling af celluloseacetatAf Kevin Beck Opdateret 24. marts 2022 Besiki Kavtaradze/iStock/GettyImages Celluloseacetat er et stof, der ligesom en række andre materialer, der anvendes i den menneskelige industri, skylder sin -
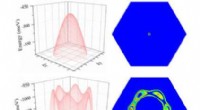 Kunne et nyt 2-D-materiale tillade, at halvledere bliver ved med at blive mindre, stærkere bedre og…I modsætning til andre materialer med elektroner, der spredes i mange retninger (nederst til venstre), elektronerne i 2D -antimon (øverst til venstre) kan fås til at bevæge sig sammen på en ordnet måd
Kunne et nyt 2-D-materiale tillade, at halvledere bliver ved med at blive mindre, stærkere bedre og…I modsætning til andre materialer med elektroner, der spredes i mange retninger (nederst til venstre), elektronerne i 2D -antimon (øverst til venstre) kan fås til at bevæge sig sammen på en ordnet måd
- Hvor godt går for tidligt fødte børn i skolen?
- Skovhabitat bliver en ørken?
- Grafenforskere skaber overophedet vand, der kan korrodere diamanter
- Hvordan blev alperne dannet af tektonisk pladebevægelse?
- Skrøbeligheds-crossover medieret af kovalent-lignende elektroniske interaktioner i metalliske væsk…
- Klima forandring, forurening og urbanisering truer vandet i Canada


