Hvordan man skriver isotoper:En simpel guide til atomnotation
Af John Brennan Opdateret 24. marts 2022
Nogle grundstoffer har kun én naturligt forekommende isotop, men andre har to, tre eller flere. Hvis du har brug for at skelne mellem de forskellige isotoper af et grundstof, kan du repræsentere hver enkelt med en simpel form for notation, der bruger massetallet, atomsymbolet og grundstoffets atomnummer. Denne notation er meget nem at lære, selvom lidt øvelse aldrig skader. Sådan skriver du isotoper for forskellige grundstoffer.
Trin 1
Slå det grundstof, du vil studere, op på det periodiske system, og kopier dets symbol ned. Symbolet for kulstof er for eksempel et stort C.
Trin 2
Find atomnummer eller protonnummer for dit grundstof. Dette giver dig antallet af protoner i dens kerne. Dette vigtige tal vises direkte over symbolet for elementet, og det vil altid være et heltal. Kulstof har for eksempel et atomnummer på 6.
Trin 3
Skriv atomnummeret som et underskrift umiddelbart foran symbolet for dit grundstof. Klik på linket under afsnittet Ressourcer, hvis du vil se, hvordan dette ser ud.
Trin 4
Skriv massetallet for din isotop som et hævet skrift umiddelbart før symbolet for grundstoffet. Massetallet går med andre ord direkte over antallet af protoner.
Ting påkrævet
- Blyant
- Papir
- Periodisk tabel
- Din isotops massenummer
TL;DR (for lang; læste ikke)
Husk at massetallet kun er antallet af protoner plus antallet af neutroner.
 Varme artikler
Varme artikler
-
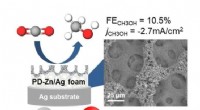 Omdannelse af kuldioxid til methanol(Venstre) Skematisk fremstilling af methanol ved elektrokatalytisk reduktion af kuldioxid ved brug af PD-Zn/Ag skumkatalysatoren. (Højre) Scanning elektronmikroskopi billede af overfladen af PD-Zn/A
Omdannelse af kuldioxid til methanol(Venstre) Skematisk fremstilling af methanol ved elektrokatalytisk reduktion af kuldioxid ved brug af PD-Zn/Ag skumkatalysatoren. (Højre) Scanning elektronmikroskopi billede af overfladen af PD-Zn/A -
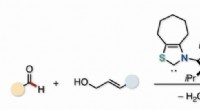 Partnere i katalyse:En effektiv vej til umættede ketonerDen samvirkende virkning af en organokatalysator og en palladiumkatalysator muliggjorde en første dehydrerende direkte allylering mellem aldehyder og allylalkoholer for at producere β, γ-umættede keto
Partnere i katalyse:En effektiv vej til umættede ketonerDen samvirkende virkning af en organokatalysator og en palladiumkatalysator muliggjorde en første dehydrerende direkte allylering mellem aldehyder og allylalkoholer for at producere β, γ-umættede keto -
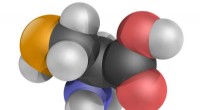 Ny dyb-læringstilgang forudsiger proteinstruktur fra aminosyresekvensAminosyren selenocystein, 3D-bolde model. Kredit:YassineMrabet/CC BY 3.0/Wikipedia Næsten alle grundlæggende biologiske processer, der er nødvendige for liv, udføres af proteiner. De skaber og ved
Ny dyb-læringstilgang forudsiger proteinstruktur fra aminosyresekvensAminosyren selenocystein, 3D-bolde model. Kredit:YassineMrabet/CC BY 3.0/Wikipedia Næsten alle grundlæggende biologiske processer, der er nødvendige for liv, udføres af proteiner. De skaber og ved -
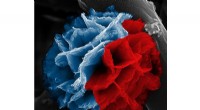 Fremstilling af rustne polymerer til energilagringDette farvede billede viser en poly (3, 4-ethylendioxythiophen) (PEDOT) nanoflower syntetiseret via hydrolyseassisteret dampfasepolymerisation ved hjælp af ethanol som opløsningsmiddel. Den blå farve
Fremstilling af rustne polymerer til energilagringDette farvede billede viser en poly (3, 4-ethylendioxythiophen) (PEDOT) nanoflower syntetiseret via hydrolyseassisteret dampfasepolymerisation ved hjælp af ethanol som opløsningsmiddel. Den blå farve
- Den kraft, du udøver på en håndtag, kaldes.?
- Hvordan kan videnskab være til gavn for miljøet?
- Er en vinterjakke eller tank fyldt med vand bedre leder af termisk energi?
- Produktvalg:Hvornår er forbrugerne mest tilfredse?
- Hvorfor er forståelse af biogeokemiske cyklusser vigtige for miljøvidenskab?
- Hvilken slags bevægelse giver lyd?


