Vands polaritet:hvorfor molekyler opfører sig som små magneter
Forestil dig at observere et enkelt vandmolekyle tæt på. Dens form ligner et bøjet "V" med oxygenatomet i spidsen og de to hydrogenatomer i vinklerne på 104,5 grader, meget som en lille, asymmetrisk magnet.
Hvorfor formen betyder noget
Vinkelgeometrien giver vand et permanent elektrisk dipolmoment:iltsiden bærer en delvis negativ ladning, mens brintsiden bærer en delvis positiv ladning. Denne polaritet er grundlaget for hydrogenbinding, den subtile, men kraftige tiltrækning mellem nabomolekyler.
Hydrogenbindinger og deres konsekvenser
I modsætning til kovalente bindinger, der låser atomer sammen, er hydrogenbindinger forholdsvis svage, men vedvarende. De gør det muligt for vand at udvise adskillige unormal adfærd, der er kritisk for livet.
Fire vigtige anomalier
Sammenhæng og overfladespænding
Vandmolekyler trækker på hinanden og skaber overfladespænding, der lader insekter gå på vandet og tillader planterødder at trække væske opad gennem kapillærer.
Forhøjet kogepunkt
At bryde hydrogenbindinger kræver betydelig energi, hvilket hæver vands kogepunkt til 100°C - meget højere end for lignende molekyler som H₂Se eller H₂S, der koger under nul. Uden dette ville Jorden ikke have noget stabilt flydende vand.
Isflydere
Når vand fryser, danner hydrogenbindinger et åbent gitter, der udvider strukturen og reducerer tætheden. Is er derfor mindre tæt end flydende vand, hvilket forhindrer vandmasser i at fryse fast og opretholder vandlevende liv om vinteren.
Universal opløsningsmiddel
Vands polaritet opløser en lang række stoffer, fra elektrolytter til organiske forbindelser, hvilket gør det uundværligt for biokemiske reaktioner og transport af næringsstoffer i levende organismer.
Praktiske konsekvenser
Mikrobølgeovne udnytter vands dipolmoment:Højfrekvent stråling justerer og agiterer dipolerne og genererer varme, der tilbereder mad effektivt. Dette er en direkte anvendelse af den samme magnetisk-lignende adfærd, der driver vands naturlige egenskaber.
Disse fænomener understreger, hvorfor vand ofte beskrives som det "universelle opløsningsmiddel" og "livsbloden" i økosystemer.
 Varme artikler
Varme artikler
-
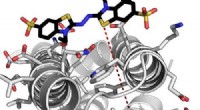 Kunstige enzymfunktioner samt naturlig versionBeregningsmodel for et yderst effektivt de novo -enzym, der interagerer med et af dets substrater. Den røde stiplede linje angiver elektrontunnelafstanden mellem det proteinbundne hæmmolekyle og det b
Kunstige enzymfunktioner samt naturlig versionBeregningsmodel for et yderst effektivt de novo -enzym, der interagerer med et af dets substrater. Den røde stiplede linje angiver elektrontunnelafstanden mellem det proteinbundne hæmmolekyle og det b -
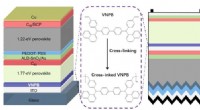 Tværbundne hultransportlag til højeffektive perovskit tandem solcellerSkematisk af perovskit/perovskite og perovskit/silicium tandem solceller. Kredit:© Science China Press Strømkonverteringseffektiviteten (PCE) for perovskite solceller med enkelt kryds (PSCer) er s
Tværbundne hultransportlag til højeffektive perovskit tandem solcellerSkematisk af perovskit/perovskite og perovskit/silicium tandem solceller. Kredit:© Science China Press Strømkonverteringseffektiviteten (PCE) for perovskite solceller med enkelt kryds (PSCer) er s -
 Drysset med kraft:Hvordan urenheder forstærker et termoelektrisk materiale på atomniveauHAXPES på Spring-8. Kredit:Dr Kotsugi I søgen efter løsninger på stadigt forværrede miljøproblemer, såsom udtømning af fossile brændstoffer og klimaændringer, mange har vendt sig til termoelektris
Drysset med kraft:Hvordan urenheder forstærker et termoelektrisk materiale på atomniveauHAXPES på Spring-8. Kredit:Dr Kotsugi I søgen efter løsninger på stadigt forværrede miljøproblemer, såsom udtømning af fossile brændstoffer og klimaændringer, mange har vendt sig til termoelektris -
 Alger puster liv i 3D-konstrueret vævEt biotrykt lobulelignende mønster indeholdende algerne, hvor tæt indkapslede celler er synlige. Til venstre er et optisk mikrofotografi, mens den højre viser et autofluorescensmikrofotografi. Kredit:
Alger puster liv i 3D-konstrueret vævEt biotrykt lobulelignende mønster indeholdende algerne, hvor tæt indkapslede celler er synlige. Til venstre er et optisk mikrofotografi, mens den højre viser et autofluorescensmikrofotografi. Kredit:
- Hvordan celler bliver uafhængige og regulerer funktioner
- Forskel mellem stjerne og vandmænd
- Vi talte med overlevende, der forbereder sig på katastrofe:her er, hvad vi lærte om verdens ende
- Diethyletherformel:Forståelse af den kemiske struktur
- Hvilken organelle er ansvarlig for at give energi til cellen?
- Hvad er forskellen mellem solenergi og termisk energi?


