Beregning af molær varmekapacitet:en praktisk vejledning
Af Riti Gupta, Opdateret 24. marts 2022
Forståelse af molær varmekapacitet er afgørende for termodynamiske beregninger. Den fortæller dig, hvor meget energi der kræves for at hæve temperaturen på et mol af et stof med en grad Celsius eller Kelvin.
Hvad er molær varmekapacitet?
Molær varmekapacitet (C) er defineret som den mængde varme, der er nødvendig for at hæve temperaturen på et mol af et stof med 1K:
C = (specific heat) × (molar mass)
Sådan beregnes det
1. Find stoffets specifikke varme (Jg⁻¹K⁻¹).
2. Gang med dens molære masse (gmol⁻¹).
Dette giver C i enheder af Jmol⁻¹K⁻¹.
Eksempel:Vand
Specifik varme for vand =4,18Jg⁻¹K⁻¹.
Molær masse af vand =18,0 gmol⁻¹.
Derfor C = 4.18 × 18.0 = 75.2 J mol⁻¹ K⁻¹ .
Eksempel:Metan (CH₄)
Specifik varme =2,20Jg⁻¹K⁻¹; molær masse =16,04 gmol-1.
Så C = 2.20 × 16.04 = 35.3 J mol⁻¹ K⁻¹ .
Brug af molær varmekapacitet til at finde varmeenergi
Den varme (q), der kræves for at ændre temperaturen, er givet af:
q = n C ΔT
• n =antal mol
• C =molær varmekapacitet (Jmol⁻¹K⁻¹)
• ΔT =temperaturændring (K)
Eksempel:Opvarmning af 5 mol kviksølv med 10K.
Specifik varme for kviksølv =27,8 Jmol⁻¹K⁻¹.
q =5mol×27,8Jmol⁻¹K⁻¹×10K =1390J.
Reversering af ligningen:Find stofmængde
Hvis du kender q, C og ΔT, kan du løse for n:
n = q / (C ΔT)
Eksempel:En calciumcarbonatprøve absorberer 550J, når dens temperatur stiger 5K, med C =82Jmol⁻¹K⁻¹.
n =550J / (82Jmol⁻¹K⁻¹×5K) =1,34mol.
Disse ligninger giver dig mulighed for at bestemme en af de fire variable – q, n, C, ΔT – når de tre andre er kendte.
 Varme artikler
Varme artikler
-
 Kaliumdrevne genopladelige batterier:En indsats mod et mere bæredygtigt miljøKalium-drevne genopladelige batteriers funktioner for et mere bæredygtigt samfund i fremtiden. Kredit:Tokyo University of Science Vores moderne livsstil ville være uhyre anderledes uden genopladel
Kaliumdrevne genopladelige batterier:En indsats mod et mere bæredygtigt miljøKalium-drevne genopladelige batteriers funktioner for et mere bæredygtigt samfund i fremtiden. Kredit:Tokyo University of Science Vores moderne livsstil ville være uhyre anderledes uden genopladel -
 Forståelse af coronavirus-varianterKredit:Pixabay/CC0 Public Domain Med fremkomsten af nye SARS-CoV-2 varianter såsom beta og delta, folk får ikke kun et genopfriskningskursus om det græske alfabet, men også oplever forvirring og
Forståelse af coronavirus-varianterKredit:Pixabay/CC0 Public Domain Med fremkomsten af nye SARS-CoV-2 varianter såsom beta og delta, folk får ikke kun et genopfriskningskursus om det græske alfabet, men også oplever forvirring og -
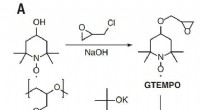 Forskere viser den højeste rapporterede ledningsevne for organisk radikal polymerDen monomersyntese og ringåbningspolymerisationsbaserede syntetiske skema, der bruges til at generere PTEO-radikalpolymeren. Kredit: Videnskab (2018). DOI:10.1126/science.aao7287 Et team af forsk
Forskere viser den højeste rapporterede ledningsevne for organisk radikal polymerDen monomersyntese og ringåbningspolymerisationsbaserede syntetiske skema, der bruges til at generere PTEO-radikalpolymeren. Kredit: Videnskab (2018). DOI:10.1126/science.aao7287 Et team af forsk -
 Perovskites – fremtidens materialer i optisk kommunikationFilmen i den nye perovskite overfører både tekst og billeder, hurtigt og pålideligt. Kredit:Thor Balkhed Forskere ved universiteterne i Linköping og Shenzhen har vist, hvordan en uorganisk perovsk
Perovskites – fremtidens materialer i optisk kommunikationFilmen i den nye perovskite overfører både tekst og billeder, hurtigt og pålideligt. Kredit:Thor Balkhed Forskere ved universiteterne i Linköping og Shenzhen har vist, hvordan en uorganisk perovsk
- Det vil snart være muligt at foretage satellittelefonopkald med din almindelige telefon
- En ny tilgang til hurtig estimering af solenergipotentialet i bymiljøer
- Sådan beregnes en spiral
- Hvad giver træer sin enorme masse i betragtning af kuldioxidvand og sollys er ikke så tunge træet…
- Hvordan celler samles og marcherer ud
- Spredning af adiabatisk justerede molekyler ved hjælp af ikke-resonante optiske stående bølger


