Hvad er en vandig opløsning? Et klart overblik
Sinhyu/iStock/GettyImages
En vandig opløsning er en blanding, hvori vand tjener som opløsningsmiddel og opløser et eller flere opløste stoffer. Mens vand oftest forekommer som en væske ved stuetemperatur, findes det også i fast (is) og gasformig (damp) tilstand.
Definition af en vandig opløsning i kemi
I kemisk notation er et stof opløst i vand markeret med endelsen (aq) . For eksempel skrives natriumchlorid i vand som NaCl(aq) , hvorimod fast salt er angivet med NaCl(s) . Dissociationen af saltet til dets bestanddele ioner er repræsenteret som Na⁺(aq) + Cl⁻(aq) .
Kun hydrofile forbindelser - dem, der tiltrækker vand - opløses let i vandige medier. Syrer, baser og mange salte falder ind under denne kategori. Hydrofobe stoffer, såsom olier og fedtstoffer, udviser begrænset opløselighed i vand.
Når elektrolytter opløses, gør de frigivne ioner opløsningen elektrisk ledende. Ikke-elektrolytter, som saccharose, forbliver intakte på molekylært niveau og leder derfor ikke elektricitet.
Hvorfor vandige opløsninger er vigtige
Vandige opløsninger er centrale i utallige kemiske processer, fra industriel syntese til biologisk funktion. I rent vand betyder mangel på ioner, at det leder elektricitet dårligt. Når først et opløst stof dissocierer til ioner, kan den resulterende elektrolytopløsning lede elektrisk strøm effektivt.
Stærke syrer og baser, såsom saltsyre eller natriumhydroxid, dissocieres fuldstændigt i vand, hvilket giver stærke elektrolytter, der forbedrer ledningsevnen. Svage elektrolytter dissocierer delvist og producerer færre frie ioner og dermed lavere ledningsevne.
Væske vs. vandig opløsning
En væske er defineret ved dens evne til at flyde, opretholde et bestemt volumen og tilpasse sin form til enhver beholder. Vand ved omgivelsestemperatur eksemplificerer disse egenskaber. En vandig opløsning er imidlertid en bestemt type væske, hvor vand er opløsningsmidlet. Mens alle vandige opløsninger er væsker, er ikke alle væsker vandige.
Nøgleegenskaber ved væsker omfatter:
- Næsten inkompressibilitet.
- Minimal densitetsændring under tryk.
- Overfladespænding, der fører til befugtningsadfærd.
- Forbedret partikelmobilitet sammenlignet med faste stoffer.
 Varme artikler
Varme artikler
-
 Forskere gennemgår de hurtige fremskridt inden for maskinlæring for de kemiske videnskaberKredit:CC0 Public Domain Et nyt værktøj ændrer ansigtet på kemisk forskning drastisk - kunstig intelligens. I et nyt blad udgivet i Natur , forskere gennemgår de hurtige fremskridt inden for mas
Forskere gennemgår de hurtige fremskridt inden for maskinlæring for de kemiske videnskaberKredit:CC0 Public Domain Et nyt værktøj ændrer ansigtet på kemisk forskning drastisk - kunstig intelligens. I et nyt blad udgivet i Natur , forskere gennemgår de hurtige fremskridt inden for mas -
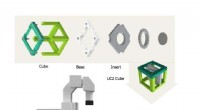 Et mikroskop for alle:Forskere udvikler open source optisk værktøjskasseDen open source 3D-printede terning kan være vært for selvdesignede indsatser, elektriske og optiske komponenter. De resulterende moduler kan kombineres til komplekse optiske instrumenter. Dette gør d
Et mikroskop for alle:Forskere udvikler open source optisk værktøjskasseDen open source 3D-printede terning kan være vært for selvdesignede indsatser, elektriske og optiske komponenter. De resulterende moduler kan kombineres til komplekse optiske instrumenter. Dette gør d -
 DESYs røntgenkilde PETRA III afslører detaljer om klæbende strukturer af edderkoppebenFor at finde ud af, hvorfor jagtedderkoppen Cupiennius salei klæber så godt til lodrette overflader, det tværfaglige forskerhold undersøger de små klæbende hår på edderkoppebenene. Kredit:Universität
DESYs røntgenkilde PETRA III afslører detaljer om klæbende strukturer af edderkoppebenFor at finde ud af, hvorfor jagtedderkoppen Cupiennius salei klæber så godt til lodrette overflader, det tværfaglige forskerhold undersøger de små klæbende hår på edderkoppebenene. Kredit:Universität -
 Nøglen til kulfrie biler? Se til stjernerneIllustration af en supernovaeksplosion. Sådanne hvirvlende masser af stof gav form til de tidligste former for kulstof - forstadier til molekyler, som nogle forskere siger, er forbundet med syntesen a
Nøglen til kulfrie biler? Se til stjernerneIllustration af en supernovaeksplosion. Sådanne hvirvlende masser af stof gav form til de tidligste former for kulstof - forstadier til molekyler, som nogle forskere siger, er forbundet med syntesen a
- Hvad er den laveste type sky i himlen?
- Video:Galileos vej til rummet
- Er Milkyway Galaxy i kollisionskursus?
- Robotter udfører Shakespeare for at lære, hvordan man redder mennesker
- Forskere siger, at frivillige virksomheders emissionsmål ikke er nok til at skabe reel klimahandlin…
- Bruger ALMA til at løse solens koronale varmemysterium


