Vandets fem essentielle egenskaber, der opretholder livet
Af Catherine Carney | Opdateret 24. marts 2022
greenaperture/iStock/GettyImages
1. Sammenhæng og vedhæftning
Vandmolekyler er polære, med en let negativ ladning på oxygenatomet og en let positiv ladning på brintatomerne. Denne polaritet skaber hydrogenbindinger - tiltrækkende kræfter mellem de modsatte ladninger af nabomolekyler. Resultatet er samhørighed (vand klæber til sig selv) og vedhæftning (vand klæber til andre hydrofile overflader). Disse egenskaber giver vand dets høje overfladespænding, hvilket muliggør fænomener såsom kapillærvirkning i planter og "klæbrighed" af en vandpyt.
2. Temperaturregulering
Vands hydrogenbinding giver det en høj specifik varme, en høj fordampningsvarme og en kraftig fordampningskølende effekt. Fordi det kræver mere energi at bryde disse bindinger, modstår vand hurtige temperaturændringer, buffer økosystemer og organismer mod ekstrem varme eller kulde. Den fordampende afkøling af sved eller transpiration er et glimrende eksempel på denne naturlige termostat.
3. Solvent Power
Polaritet gør også vand til et fremragende opløsningsmiddel for andre polære eller hydrofile molekyler. Det opløser let salte, sukkerarter og mange biologiske makromolekyler, hvilket letter utallige biokemiske reaktioner. I modsætning hertil forbliver ikke-polære, hydrofobe stoffer såsom olier stort set uopløste og danner adskilte faser.
4. Densitetsanomali – Ekspansion ved frysning
I modsætning til de fleste væsker udvider vandet sig, når det fryser. Det stive gitter dannet af hydrogenbindinger optager mere volumen end væskearrangementet, så is er mindre tæt end flydende vand. Dette får is til at flyde, isolerer vandområder og bevarer vandlevende liv i kolde årstider.
5. Neutral pH
Rent vand dissocieres i nogenlunde lige store koncentrationer af H⁺- og OH⁻-ioner, hvilket giver en neutral pH-værdi på 7. Denne neutralitet gør det muligt for det at tjene som en buffer i biologiske systemer og tilpasse sig let sure eller basiske forhold, som kræves af forskellige enzymer.
Disse fem indbyrdes forbundne egenskaber – kohæsion/adhæsion, temperaturstabilitet, opløsningsmiddelevne, ekspansion ved frysning og neutral pH – gør vand til hjørnestenen i alt kendt liv.
 Varme artikler
Varme artikler
-
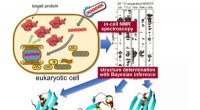 In-situ måling af 3-D proteinstruktur inde i levende eukaryote cellerMålproteiner udtrykkes indeni sf9 celler, derefter målt under anvendelse af in-cell NMR-spektroskopi. Unik statistisk analyse ved hjælp af Bayesiansk slutning anvendes til at beregne den nøjagtige
In-situ måling af 3-D proteinstruktur inde i levende eukaryote cellerMålproteiner udtrykkes indeni sf9 celler, derefter målt under anvendelse af in-cell NMR-spektroskopi. Unik statistisk analyse ved hjælp af Bayesiansk slutning anvendes til at beregne den nøjagtige -
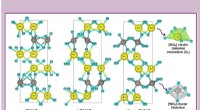 Forskere forbedrer syntesen af bismuth-wolframat med en miljøvenlig procedureKredit:Asociación RUVID Et tværfagligt forskerhold fra Universitat Jaume I (UJI) i samarbejde med Center for Development of Functional Materials (CDMF) i Brasilien har for første gang vist den eff
Forskere forbedrer syntesen af bismuth-wolframat med en miljøvenlig procedureKredit:Asociación RUVID Et tværfagligt forskerhold fra Universitat Jaume I (UJI) i samarbejde med Center for Development of Functional Materials (CDMF) i Brasilien har for første gang vist den eff -
 Strategisk formulering af almindelig cement kan have stor indflydelse på vandrensningÅbne kanaler, der fører vand, kan laves med en ny cementformulering, der vil rense vandet via soleksponering, når det strømmer mod sin destination. Kredit:U.S. Geological Survey Department of the Inte
Strategisk formulering af almindelig cement kan have stor indflydelse på vandrensningÅbne kanaler, der fører vand, kan laves med en ny cementformulering, der vil rense vandet via soleksponering, når det strømmer mod sin destination. Kredit:U.S. Geological Survey Department of the Inte -
 Udvikling af en måde at gøre oxygen injicerbarJarad Mason og hans team har skabt permanent porøst vand, hvilket gør det muligt at opbevare gasser i høje koncentrationer i væsken. Kredit:Kris Snibbe/Harvard Staff Photographer Hvad hvis akutmedi
Udvikling af en måde at gøre oxygen injicerbarJarad Mason og hans team har skabt permanent porøst vand, hvilket gør det muligt at opbevare gasser i høje koncentrationer i væsken. Kredit:Kris Snibbe/Harvard Staff Photographer Hvad hvis akutmedi


