Forståelse af atomer og molekyler:nøgleforskelle forklaret
Af Natasha Gilani – Opdateret marts242022
Fysisk stof er konstrueret af atomer og molekyler. Et atom er den mindste enhed af et grundstof, mens et molekyle er en samling atomer forbundet med kemiske bindinger - ioniske, kovalente eller metalliske.
Egenskaber
Atomer kan være neutrale, have lige mange protoner og elektroner eller ladet som ioner. En positiv ion har flere protoner end elektroner; en negativ ion har flere elektroner. Antallet af protoner definerer atomnummeret (Z), neutroner giver neutrontallet (N), og massetallet (A) er lig med Z+N. Molekyler, som generelt er neutrale, kan eksistere i stabile eller ustabile former, og deres masse er afledt af summen af deres konstituerende atomer.
Komponenter
Et atom består af en kerne - der indeholder protoner (positiv ladning) og neutroner (neutrale) - og en elektronsky. Elektroner, med en masse omkring 0,0005 af en proton, kredser om kernen. Kernen tegner sig for omkring 99,9% af et atoms masse. Et molekyle er lavet af to eller flere atomer bundet sammen af en stærk kemisk binding.
Størrelse
Atomer er omtrent 0,2 nanometer (2×10⁻¹⁰m) på tværs. Det mindste naturlige molekyle, diatomisk hydrogen (H₂), måler 0,74Å (7,4×10⁻¹¹m).
Form
Atomer mangler en fast form, der fremstår som kugler, lapper eller ringe. Geometrien af et molekyle afhænger af, hvordan dets atomer er arrangeret. Almindelige former inkluderer lineære, trigonale plane, tetraedriske, trigonale pyramideformede, trigonale bipyramidale og oktaedriske. For eksempel er et diatomisk molekyle lineært, mens BF₃ antager en trigonal plan form med 120-graders F–B–F-vinkler.
Typer
Atomer varierer efter størrelse, masse og identitet - hydrogen, svovl, oxygen, nitrogen osv. Molekyler klassificeres som diatomiske (to atomer), homoatomiske (to eller flere atomer af samme grundstof) eller heteroatomiske (atomer af forskellige grundstoffer). Simple molekyler indeholder et enkelt atom; komplekse molekyler består af flere atomer.
 Varme artikler
Varme artikler
-
 Drysset med kraft:Hvordan urenheder forstærker et termoelektrisk materiale på atomniveauHAXPES på Spring-8. Kredit:Dr Kotsugi I søgen efter løsninger på stadigt forværrede miljøproblemer, såsom udtømning af fossile brændstoffer og klimaændringer, mange har vendt sig til termoelektris
Drysset med kraft:Hvordan urenheder forstærker et termoelektrisk materiale på atomniveauHAXPES på Spring-8. Kredit:Dr Kotsugi I søgen efter løsninger på stadigt forværrede miljøproblemer, såsom udtømning af fossile brændstoffer og klimaændringer, mange har vendt sig til termoelektris -
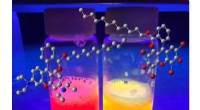 Lab producerer simple fluorescerende overfladeaktive stofferRice University kemikere har produceret en række fluorescerende overfladeaktive stoffer til billeddannelse, biomedicinske og fremstillingsapplikationer. Kredit:Ashleigh Smith McWilliams/Rice Universit
Lab producerer simple fluorescerende overfladeaktive stofferRice University kemikere har produceret en række fluorescerende overfladeaktive stoffer til billeddannelse, biomedicinske og fremstillingsapplikationer. Kredit:Ashleigh Smith McWilliams/Rice Universit -
 Surrey bygger AI til at finde kemiske forbindelser mod ældningKredit:CC0 Public Domain University of Surrey har opbygget en kunstig intelligens (AI) model, der identificerer kemiske forbindelser, der fremmer sund aldring - og baner vejen mod farmaceutiske in
Surrey bygger AI til at finde kemiske forbindelser mod ældningKredit:CC0 Public Domain University of Surrey har opbygget en kunstig intelligens (AI) model, der identificerer kemiske forbindelser, der fremmer sund aldring - og baner vejen mod farmaceutiske in -
 Ultratynde lag af rust genererer elektricitet fra strømmende vandKredit:Morteza Akhnia/Unsplash Der er mange måder at generere elektricitet på – batterier, solpaneler, vindturbine, og vandkraftdæmninger, for at nævne et par eksempler... og nu, der er rust. Ny
Ultratynde lag af rust genererer elektricitet fra strømmende vandKredit:Morteza Akhnia/Unsplash Der er mange måder at generere elektricitet på – batterier, solpaneler, vindturbine, og vandkraftdæmninger, for at nævne et par eksempler... og nu, der er rust. Ny
- NASA beregner Tropical Storm Harveys oversvømmende nedbør
- Loess Dunes and Moraines er eksempler på hvad?
- Hvad giver meteoritter deres form? Ny forskning afslører et Guldlok-svar
- Plantemateriale på obsidianblade på Rapa Nui tyder på, at bosættere der besøgte Sydamerika og v…
- Forskere opdager usædvanlig konkurrence mellem ladningstæthedsbølge og superledning
- Navngiv de 3 molekyler involveret i oversættelsesprocessen?


