Atomer og molekyler:Hvordan de forbindes for at opbygge alt stof
Af Jess Kroll Opdateret 24. marts 2022
Atomer
Atomer er de grundlæggende byggesten i livet og alt andet. Hvert atom indeholder en tæt kerne af protoner og neutroner, omgivet af en sky af elektroner. Protoner har en positiv ladning, elektroner en negativ ladning, og neutroner er elektrisk neutrale. Et grundstofs atomvægt er summen af dets protoner og neutroner, mens atomnummeret - altid antallet af protoner - identificerer grundstoffet. Fordi protontallet aldrig ændres, arrangerer det periodiske system grundstoffer ved at øge atomnummeret, begyndende med brint (1p, 1e) og strækker sig til radium (88p, 88e).
Molekyler
Et molekyle er enhver gruppe af to eller flere atomer bundet sammen for at danne et særskilt kemisk stof. Almindelige eksempler omfatter vand (H2O), kuldioxid (CO2) og dioxygen (O2). Den kemiske formel angiver både de involverede typer atomer og deres relative antal. Fjernelse af et atom fra et molekyle ændrer fundamentalt dets identitet; et vandmolekyle mister sine egenskaber, hvis det mister et iltatom.
Kemiske bindinger
Atomer forbliver sammen gennem kemiske bindinger, tiltrækningen mellem de positivt ladede kerner og de negativt ladede elektroner. Bindinger kan være kovalente - hvor elektroner deles - eller ioniske, hvor elektroner overføres. I vand deler oxygenatomet elektroner med to brintatomer, hvilket skaber et polært molekyle med en delvis negativ ladning på ilt og en delvis positiv ladning på brint, hvilket understøtter vands unikke egenskaber.
Forbindelser
Forbindelser opstår, når atomer af to eller flere forskellige grundstoffer forbindes i et fast forhold. Mangfoldigheden af mulige forbindelser er i det væsentlige grænseløs, selvom der kun er 118 kendte grundstoffer. For eksempel er ethanol (C2H5OH) en alkohol, hvor et carbonatom er bundet til en hydroxylgruppe. Det specifikke arrangement af atomer – i stedet for blot de tilstedeværende grundstoffer – bestemmer en forbindelses egenskaber.
Enkeltelementsforbindelser
Nogle stoffer består af et enkelt grundstof, men i forskellige molekylære former. Molekylær oxygen (O₂) er essentiel for respiration, hvorimod ozon (O₃) beskytter planeten mod ultraviolet stråling, men kan være skadelig for levende væv. Antallet af atomer i molekylet ændrer dets adfærd og rolle i naturen.
 Varme artikler
Varme artikler
-
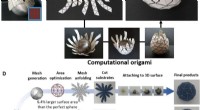 Computational origami:En universel metode til at indpakke 3-D buede overflader med ikke-strækbare m…Reverse engineering computerorigami til konform indpakning. (A) Rynker dannes ved tæt indpakning af et rektangulært ark papir omkring en ikke -nul Gauss -overflade. (B) Fraktale snitmønstre kan undgå
Computational origami:En universel metode til at indpakke 3-D buede overflader med ikke-strækbare m…Reverse engineering computerorigami til konform indpakning. (A) Rynker dannes ved tæt indpakning af et rektangulært ark papir omkring en ikke -nul Gauss -overflade. (B) Fraktale snitmønstre kan undgå -
 Dens regnende diamanter over hele universet, tyder forskning påUranus og Neptun, isgiganter, hvor videnskabsmænd mener, at diamantregn falder under overfladen. Det kan regne med diamanter på planeter i hele universet, foreslog videnskabsmænd fredag, efter at h
Dens regnende diamanter over hele universet, tyder forskning påUranus og Neptun, isgiganter, hvor videnskabsmænd mener, at diamantregn falder under overfladen. Det kan regne med diamanter på planeter i hele universet, foreslog videnskabsmænd fredag, efter at h -
 Forskere udvikler en ny heterostrukturkatalysator til effektiv brintgenerering fra vandspaltningAC Transit brint brændselscelle bus. Kredit:Eric Fischer. Bekymringer om stigende atmosfæriske kuldioxidniveauer og global opvarmning har gjort det til en miljømæssig nødvendighed at erstatte fossi
Forskere udvikler en ny heterostrukturkatalysator til effektiv brintgenerering fra vandspaltningAC Transit brint brændselscelle bus. Kredit:Eric Fischer. Bekymringer om stigende atmosfæriske kuldioxidniveauer og global opvarmning har gjort det til en miljømæssig nødvendighed at erstatte fossi -
 Silkemikrokokoner kunne bruges i bioteknologi og medicinSilkeormen spinder en silkekokon rundt om sig selv for at beskytte sig under metamorfosen. Forskere har fundet ud af, at silke kan beskytte andre dyrebare laster. Kredit:2017 Natural Materials Group
Silkemikrokokoner kunne bruges i bioteknologi og medicinSilkeormen spinder en silkekokon rundt om sig selv for at beskytte sig under metamorfosen. Forskere har fundet ud af, at silke kan beskytte andre dyrebare laster. Kredit:2017 Natural Materials Group
- Ny teknologi har til formål at forbedre litiummetalbatteriets levetid, sikkerhed
- Hvad menes med neutrale gasser?
- Hvad er værdien af en halv skilling fra 1911 med stjerner?
- Hvad er opbygningen og nedbrydning af kemikalier i celle?
- Er gasplaneter frosset som iskrystaller?
- Hvilken type energiændring i en højttaler?


