Konvertering af damptryk til gaskoncentration:en praktisk vejledning
Af Shawn Radcliffe
Opdateret 24. marts 2022
IvanMikhaylov/iStock/GettyImages
Selv når en væske ser ud til at være stille, fordamper molekyler i den konstant til luften ovenover og kondenserer tilbage igen. Når disse modsatrettede processer balancerer, når systemet ligevægt. Ved ligevægt afspejler dampens partialtryk direkte dens koncentration i gasfasen. For at omsætte dette tryk til en målbar koncentration anvender vi den ideelle gaslov, som forbinder tryk, temperatur og molær mængde.
Trin 1:Skriv den ideelle gaslov
Den ideelle gasligning er PV =nRT , hvor:
- P =tryk (atm)
- V =volumen (L)
- n =antal mol
- T =temperatur (K)
- R =universel gaskonstant =0,0821 latmmol⁻¹K⁻¹
Trin 2:Løs for koncentration (n/V)
Omarranger ligningen for at isolere molaritet:
n/V =P/(RT)Koncentrationen er således lig med partialtrykket divideret med produktet af gaskonstanten og temperaturen.
Trin 3:Konverter temperatur til Kelvin
Brug relationen K =°C + 273,15 . For eksempel bliver 25°C til 298K.
Trin 4:Konverter tryk til atmosfærer
Hvis din måling er i torr, skal du gange med 0,001316 for at opnå atmosfærer. For eksempel, 25torr =0,0329atm.
Trin 5:Beregn koncentrationen
Indsæt de konverterede værdier i ligningen. Med en temperatur på 298K og et partialtryk på 0,031 atm:
n/V =0,031 / (0,0821 × 298) ≈ 0,0013molL⁻¹Dette resultat udtrykker dampkoncentrationen som 1,3×10⁻³mol pr. liter.
TL;DR
Ved ligevægt er en gass koncentration lig med dens partialtryk. Konverter temperatur til Kelvin og tryk til atmosfærer, og anvend derefter n/V =P/(RT) for at opnå molariteten.
 Varme artikler
Varme artikler
-
 Gennem tykt og tyndt:Neutroner sporer lithium-ioner i batterielektroderKemiingeniørforskere fra University of Virginia School of Engineering anvender neutronbilleddannelse ved Oak Ridge National Laboratory til at undersøge lithium-ion-batterimaterialer og -strukturer. Kr
Gennem tykt og tyndt:Neutroner sporer lithium-ioner i batterielektroderKemiingeniørforskere fra University of Virginia School of Engineering anvender neutronbilleddannelse ved Oak Ridge National Laboratory til at undersøge lithium-ion-batterimaterialer og -strukturer. Kr -
 At bryde grænsen for kemiske forbindelserKredit:CC0 Public Domain Siden slutningen af det 19. århundrede, overgangsmetalcarbonyler har været en vigtig og velkendt klasse af forbindelser inden for koordinationskemi og organometallisk ke
At bryde grænsen for kemiske forbindelserKredit:CC0 Public Domain Siden slutningen af det 19. århundrede, overgangsmetalcarbonyler har været en vigtig og velkendt klasse af forbindelser inden for koordinationskemi og organometallisk ke -
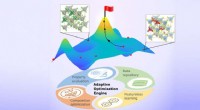 Ny tilgang bestemmer optimale materialedesign med minimale dataKredit:Northwestern University Northwestern University-forskere har udviklet en ny beregningsmæssig tilgang til at accelerere designet af materialer, der udviser metal-isolator overgange (MIT), en
Ny tilgang bestemmer optimale materialedesign med minimale dataKredit:Northwestern University Northwestern University-forskere har udviklet en ny beregningsmæssig tilgang til at accelerere designet af materialer, der udviser metal-isolator overgange (MIT), en -
 Belysning af måden at skifte kemiske reaktionsvejeForskere brugte grøn laser til at modulere reaktiviteten af triazolinediones (TADer), kraftfulde kemiske koblingsmidler. Kredit:QUT Kunne fremstillingen af de integrerede kredsløb og chips til
Belysning af måden at skifte kemiske reaktionsvejeForskere brugte grøn laser til at modulere reaktiviteten af triazolinediones (TADer), kraftfulde kemiske koblingsmidler. Kredit:QUT Kunne fremstillingen af de integrerede kredsløb og chips til
- Hvad er bølgelængde på frekvens 20Hz?
- Hvordan forbedrer solreflektorer effektiviteten af samler?
- Ud i det blå:Hvordan bardehvaler har tilpasset sig gennem de sidste 50 millioner år
- Skolen er ude:hvordan klimaændringer truer uddannelse
- NASA-NOAA satellit sporer Isaias udvikling, bevægelse, gennemblødningspotentiale
- Er sandbjælker dannet af erosionsbølger?


