Kobber og salpetersyre:Forståelse af oxidations-reduktionsreaktioner
By John Brennan Updated Mar 24, 2022
Sinhyu/iStock/GettyImages
Reaktionerne mellem kobber og salpetersyre er eksempler på oxidations-reduktionsreaktioner, hvor at få elektroner reducerer det ene grundstof, og at miste dem oxiderer det andet. Salpetersyre er ikke kun en stærk syre, det er et oxidationsmiddel. Derfor kan det oxidere kobber til Cu+2. Hvis du planlægger at eksperimentere med disse reaktioner, er det vigtigt at huske, at de frigiver giftige, skadelige dampe.
Solution Concentration
Løsningskoncentration
Kobber kan gennemgå en af to reaktioner, når det kombineres med salpetersyre, afhængigt af opløsningens koncentration. Hvis salpetersyren er fortyndet, vil kobberet blive oxideret til dannelse af kobbernitrat med nitrogenoxid som et biprodukt. Hvis opløsningen er koncentreret, vil kobberet blive oxideret til dannelse af kobbernitrat med nitrogendioxid som et biprodukt. Både nitrogenoxid og nitrogendioxid er skadelige og potentielt giftige ved høje niveauer; nitrogendioxid er den grimme brune gas, der findes i smogdisen over mange byer.
Reaction Equations
Reaktionsligninger
Ligningerne for de to reaktioner, der kan finde sted, er:
Cu + 4 HNO3 –> Cu(NO3)2 + 2 NO2 + 2 H2O, som producerer nitrogendioxid og
3 Cu + 8 HNO3 –> 3 Cu(NO3)2 + 2 NO + 4 H2O, som producerer nitrogenoxid.
Med den koncentrerede syre bliver opløsningen først grøn, derefter grønlig-brun og til sidst blå, når den er fortyndet med vand. Begge reaktioner er meget eksoterme og frigiver energi i form af varme.
Oxidation and Reduction
Oxidation og reduktion
En anden måde at forstå denne reaktion på er ved at opdele den i to halvreaktioner, den ene til oxidation (tab af elektroner) og den anden til reduktion (forstærkning af elektroner). Halvereaktionerne er:Cu –> Cu2+ + 2 e-, hvilket betyder, at kobber mister to elektroner, og 2 e- + 4 HNO3 —> 2 NO3 1- + 2 H2O, hvilket viser, at to elektroner er blevet overført til produkterne. Hastigheden af denne reaktion afhænger af kobberets overfladeareal; kobbertråd vil reagere hurtigere end f.eks. kobberstænger.
Other Considerations
Andre overvejelser
The solution changes color because of the water. I modsætning til kobberfaststoffet kan kobberionerne i opløsning danne en type interaktion kaldet et koordinationskompleks med vandmolekylerne, og disse komplekser giver opløsningen en blå farve. Mineralsyrer som saltsyre oxiderer ikke kobber på samme måde som salpetersyre, fordi de ikke er stærke oxidationsmidler. Svovlsyre er imidlertid et stærkt oxidationsmiddel. Under de rette forhold vil det reagere med kobber for at frigive svovldioxidgas.
 Varme artikler
Varme artikler
-
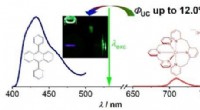 En ny vej til bæredygtig fotonopkonvertering med ikke-ædelmetallerDen molekylære rubin [Cr(bpmp)2 ]3+ med en jordrig chrom(III) central ion sensibiliserer grøn-til-blå triplet-triplet annihilation opkonvertering med 9,10-diphenylanthracen som annihilator. Processen
En ny vej til bæredygtig fotonopkonvertering med ikke-ædelmetallerDen molekylære rubin [Cr(bpmp)2 ]3+ med en jordrig chrom(III) central ion sensibiliserer grøn-til-blå triplet-triplet annihilation opkonvertering med 9,10-diphenylanthracen som annihilator. Processen -
 Nye stoffer med antivirale egenskaberKredit:CC0 Public Domain Brasilianske tekstilvirksomheder er begyndt at producere og markedsføre stoffer behandlet med sølv- og silica -nanopartikler udviklet af forskningsgrupperne ved Center for
Nye stoffer med antivirale egenskaberKredit:CC0 Public Domain Brasilianske tekstilvirksomheder er begyndt at producere og markedsføre stoffer behandlet med sølv- og silica -nanopartikler udviklet af forskningsgrupperne ved Center for -
 At opnå stærke strukturer med kulfiberforstærket plastEn fejl på grund af den klassiske globale knækning af søjlen med begge endestifter opleves af den ustyrkede kontrolprøve, (en). Sammenlignet med formen af kontrolprøverne, den deformerede form af al
At opnå stærke strukturer med kulfiberforstærket plastEn fejl på grund af den klassiske globale knækning af søjlen med begge endestifter opleves af den ustyrkede kontrolprøve, (en). Sammenlignet med formen af kontrolprøverne, den deformerede form af al -
 Bygninger – Beton på det dobbelteORNL forskere brugte fiberforstærkninger lavet af stål, glas og kulstof for at udvikle en betonblanding, der viste høj tidlig styrke inden for seks timer efter produktion, som er nødvendig for den præ
Bygninger – Beton på det dobbelteORNL forskere brugte fiberforstærkninger lavet af stål, glas og kulstof for at udvikle en betonblanding, der viste høj tidlig styrke inden for seks timer efter produktion, som er nødvendig for den præ
- Hvilken energi opbevares inden for atomer?
- Hvor mange oz i en 375 ml flaske?
- Hvilken rolle spiller konkurrence i teorien om naturlig udvælgelse?
- Kalium i gasform:Forståelse af dets egenskaber og adfærd
- IMERG tilføjer kraftig nedbør fra Tropical Storm Damrey
- En gas består af en blanding af neon og argon rms hastighed atomerne er 350 hvad atomer?


