Hvad bestemmer en syres styrke? En klar guide til protondissociation
Foto:iStock/GettyImages
Det definerende træk ved en syre er opførselen af dens brintatomer, når de er opløst i vand. En stærk syre frigiver de fleste, hvis ikke alle, af sine brintatomer som frie protoner, som straks binder sig til vandmolekyler og danner hydroniumioner (H₃O⁺). Den resterende del af syremolekylet bliver den konjugerede base, der bærer en negativ ladning. Den grad, hvormed denne dissociation sker, bestemmer syrens styrke.
TL;DR
Stærke syrer ioniserer fuldstændigt, producerer hydroniumioner og efterlader den konjugerede base som en negativ ion. Svage syrer forbliver stort set udissocierede, hvor kun en lille del afgiver protoner. Balancen mellem disse arter giver syrer deres karakteristiske adfærd.
Stærke syrer og deres dissociation
De mest almindeligt forekommende stærke syrer er saltsyre (HCl) og svovlsyre (H2SO4). I saltsyre er H-Cl-bindingen så svag, at hvert brintatom løsnes, når syren opløses. Den frigjorte proton bliver til en hydroniumion, mens chloridionen bærer en ladning -1.
I svovlsyre er begge hydrogenatomer tilsvarende svagt bundet. Ved opløsning danner de to protoner to hydroniumioner, og den resterende SO4²⁻-enhed bærer en ladning -2. På grund af denne fuldstændige dissociation er begge syrer yderst effektive til at protonere andre stoffer.
Stærke baser og deres dissociation
Stærke baser opfører sig på den modsatte måde:de frigiver hydroxidioner (OH⁻) i stedet for protoner. Natriumhydroxid (NaOH) og calciumhydroxid (Ca(OH)2) er klassiske eksempler. Hvert molekyle spalter fuldstændigt i vand, hvilket giver en høj koncentration af OH⁻, der giver opløsningen grundlæggende karakter.
Neutralisering af stærke syrer og baser
Når en stærk syre og en stærk base mødes, parrer deres ioner sig fuldstændigt. H⁺ fra syren kombineres med OH⁻ fra basen for at danne vand, mens de resterende ioner samles til et neutralt salt. For eksempel producerer tilsætning af NaOH til HCl vand og natriumchlorid (NaCl), et stabilt, neutralt salt. Fuldstændigheden af ionisering tillader disse reaktioner at fortsætte til fuldførelse under normale forhold.
 Varme artikler
Varme artikler
-
 Lille, men selvpålagt:Titanium ændrer værtsgitteratoms adfærdTitan, gitterets herre. Kredit:Daria Sokol, MIPT Forskere fra MIPT og deres kolleger fra Ural Federal University har kombineret optiske og akustiske tilgange og fundet ud af, at inkorporering af t
Lille, men selvpålagt:Titanium ændrer værtsgitteratoms adfærdTitan, gitterets herre. Kredit:Daria Sokol, MIPT Forskere fra MIPT og deres kolleger fra Ural Federal University har kombineret optiske og akustiske tilgange og fundet ud af, at inkorporering af t -
 Styring af zeolitporenes indre til kemo-selektive alkyn/olefin-separationerAdsorptionsdata for C2H2 og C2H4 for Ni@FAU. (A) Adsorptionsisotermer af C2H2 og C2H4 for Ni@FAU ved 298 K. STP, standard temperatur og tryk. (B) TPD-profiler af C2H2- og C2H4-adsorberet Ni@FAU efter
Styring af zeolitporenes indre til kemo-selektive alkyn/olefin-separationerAdsorptionsdata for C2H2 og C2H4 for Ni@FAU. (A) Adsorptionsisotermer af C2H2 og C2H4 for Ni@FAU ved 298 K. STP, standard temperatur og tryk. (B) TPD-profiler af C2H2- og C2H4-adsorberet Ni@FAU efter -
 Forskere undersøgte fremstillingen af polymerfibre til brug i avanceret sundhedsplejeMohan Edirisinghe leder et team på University College London, der studerer fremstillingen af polymere nanofibre og mikrofibre - meget tynde fibre, der består af polymerer. Fibrene kan væves ind i te
Forskere undersøgte fremstillingen af polymerfibre til brug i avanceret sundhedsplejeMohan Edirisinghe leder et team på University College London, der studerer fremstillingen af polymere nanofibre og mikrofibre - meget tynde fibre, der består af polymerer. Fibrene kan væves ind i te -
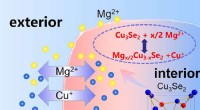 Kobberion låser op for magnesium potentiale i næste generations batterierVed at tilføje en kobberion, nyt magnesiumbatteri demonstrerer dramatisk forbedring af ydeevnen. Kredit:CUI Guanglei Forskere ved Qingdao Institute of Bioenergy and Bioprocess Technology (QIBEBT)
Kobberion låser op for magnesium potentiale i næste generations batterierVed at tilføje en kobberion, nyt magnesiumbatteri demonstrerer dramatisk forbedring af ydeevnen. Kredit:CUI Guanglei Forskere ved Qingdao Institute of Bioenergy and Bioprocess Technology (QIBEBT)
- Breakthrough Listen udgiver katalog over Exotica - objekter af interesse som teknosignaturer
- Er en ny stjerne kaldet protostar?
- Top fransk filosof advarer mod virusudnyttelse
- Hvorfor er en bromidion større end bromatom?
- Hvilken engelsk videnskabsmand fra det nittende århundrede fremlagde bevis for, at atomer eksistere…
- Er H2O2 n grundstof sammensat eller blanding?


