Sådan bestemmes neutroner, protoner og elektroner i atomer, ioner og isotoper
Af Riti Gupta – Opdateret 24. marts 2022
Når du skal identificere den subatomære sammensætning af enhver kemisk art, er det periodiske system din primære reference. Nedenfor er en klar guide til, hvordan man udvinder antallet af neutroner, protoner og elektroner for neutrale atomer, ladede ioner og isotoper ved hjælp af det periodiske system og nuklear notation.
Læsning af det periodiske system
Det periodiske system indeholder al den information, du har brug for om et grundstofs subatomare struktur:
- Symbol – Den elementære stenografi (f.eks. C for kulstof).
- Atomnummer (Z) – Placeret over symbolet er det lig med antallet af protoner og, for et neutralt atom, antallet af elektroner. For kulstof,
Z = 6. - Atommasse – Under symbolet et vægtet gennemsnit af alle naturlige isotoper. Når det afrundes til nærmeste hele tal, svarer det til massetallet for den mest udbredte isotop. For kulstof giver dette et massetal
M = 12, som er summen af protoner og neutroner.
For at finde antallet af neutroner i et neutralt atom skal du trække atomnummeret fra massetallet:
#neutrons = M – Z – For kulstof, 12 – 6 = 6 neutroner.
Beregning af subatomære partikler i ioner
Ioner dannes, når et atom får eller taber elektroner, hvilket ændrer dets samlede ladning. Overskriften på ionsymbolet angiver nettoladningen. For eksempel Cl – er en chloridion med en ladning -1.
Bestem først det neutrale atoms proton- og neutrontal fra det periodiske system. Klor har Z = 17 protoner og ved hjælp af M = 35 , #neutrons = 35 – 17 = 18 neutroner.
Fordi ionen bærer en negativ ladning, indeholder den en ekstra elektron. Brug ladningsbalanceligningen:
#e– + #p+ = charge
Erstatning af kendte værdier for chlorid:
#e– + 17 = –1 → #e– = 18
Således Cl – indeholder 17 protoner, 18 neutroner og 18 elektroner.
Identifikation af subatomære partikler i isotoper
Isotoper er varianter af det samme grundstof, der kun adskiller sig i neutrontal. Nuklear notation er en kortfattet måde at repræsentere dem på. For eksempel skrives kulstof-12 som ¹²⁶C .
I nuklear notation:
- Symbol – Elementets symbol (C).
- Massetal (A) – Det hævede skrift (12) er lig med protoner + neutroner.
- Atomnummer (Z) – Sænkningen (6) er protontallet, konstant for elementet.
For at finde neutrontallet for en specifik isotop skal du løse:
#neutrons + Z = A
For kulstof-13 (¹³⁶C ):
#neutrons + 6 = 13 → #neutrons = 7
Derfor har kulstof-13 6 protoner, 7 neutroner og, hvis neutral, 6 elektroner. Carbon-12 har 6 protoner, 6 neutroner og 6 elektroner.
Ved at kombinere periodiske tabeldata med nuklear notation kan du nøjagtigt bestemme den subatomare sammensætning af ethvert atom, ion eller isotop.
 Varme artikler
Varme artikler
-
 Forskere ved ESS, Svensk vandforskning, ORNL bruger VISION til at se på almindelige forurenende sto…Brug af neutronspredning, Monika Hartl fra European Spallation Source studerer, hvordan vandfiltre interagerer med forurenende stoffer for at optimere filterdesign og forbedre vandbehandlingsmetoder.
Forskere ved ESS, Svensk vandforskning, ORNL bruger VISION til at se på almindelige forurenende sto…Brug af neutronspredning, Monika Hartl fra European Spallation Source studerer, hvordan vandfiltre interagerer med forurenende stoffer for at optimere filterdesign og forbedre vandbehandlingsmetoder. -
 Guldbelagte strømpebukser inspirerer til en teknik til behageligt lysemitterende tøjDisse fotografier viser lysemitterende tekstiler, der viser emojien smilende ansigt, en rektangulær spiral, og tallet 8. Kredit:The Carmichael Lab En fremgangsmåde til udvikling af lysemitterende
Guldbelagte strømpebukser inspirerer til en teknik til behageligt lysemitterende tøjDisse fotografier viser lysemitterende tekstiler, der viser emojien smilende ansigt, en rektangulær spiral, og tallet 8. Kredit:The Carmichael Lab En fremgangsmåde til udvikling af lysemitterende -
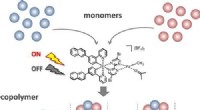 Brugerdefinerede sekvenser til polymerer ved hjælp af synligt lysBrugerdefineret sekvens af forskellige sammensætninger i en enkelt polymerkæde, skabt ved blot at udsætte en igangværende polymerisationsreaktion for forskellige tænd/sluk-sekvenser af synligt lys. Kr
Brugerdefinerede sekvenser til polymerer ved hjælp af synligt lysBrugerdefineret sekvens af forskellige sammensætninger i en enkelt polymerkæde, skabt ved blot at udsætte en igangværende polymerisationsreaktion for forskellige tænd/sluk-sekvenser af synligt lys. Kr -
 Fire typer orbitaler og deres former – en praktisk vejledningAf Richard Gaughan Opdateret 30. august 2022 twilightproductions/iStock/GettyImages Atomer består af en tung kerne omgivet af lette elektroner. Kvantemekanikken dikterer, at elektroner optager forsk
Fire typer orbitaler og deres former – en praktisk vejledningAf Richard Gaughan Opdateret 30. august 2022 twilightproductions/iStock/GettyImages Atomer består af en tung kerne omgivet af lette elektroner. Kvantemekanikken dikterer, at elektroner optager forsk
- Det sydlige Ocean har den reneste luft på Jorden - videnskabsmænd har netop opdaget hvorfor
- Hvad er miner?
- Hvad er oxidationstallet for gruppe 5?
- Nogle kovalente forbindelser adskiller sig i ioner, når de opløses i vand 1 Hvad atomer gør disse…
- Forskere udvikler en billig, målrettet antibakteriel forbindelse
- Hvad kredserer jorden og tager billeder af den?


