Fire typer orbitaler og deres former – en praktisk vejledning
Af Richard Gaughan Opdateret 30. august 2022
twilightproductions/iStock/GettyImages
Atomer består af en tung kerne omgivet af lette elektroner. Kvantemekanikken dikterer, at elektroner optager forskellige områder kaldet orbitaler. Fordi kemiske interaktioner primært sker gennem de yderste elektroner, er formen af disse orbitaler afgørende for at forstå, hvordan atomer binder sig og opfører sig.
Kvantumal og orbitaler
Fysikere beskriver en elektrons tilstand med et sæt heltalske kvantetal. Det primære kvantetal n relaterer sig til energi, mens orbital kvantetal l og det magnetiske kvantetal m bestemme orbitalens geometri og orientering. Der findes yderligere kvantetal, men de har ikke direkte indflydelse på orbitalformen. Orbitaler repræsenterer sandsynlighedsskyer – ikke bogstavelige elektronbaner – rundt om kernen.
S orbitaler
For hver værdi af n , er der én orbital, hvor begge l og m lig nul. Disse er sfæriske skaller, der udvides i størrelse som n stiger. S-kredsløbet er den eneste type, der eksisterer for grundtilstanden (n=1) og optræder i hvert hovedenerginiveau. Selvom elektrontætheden er højere nær kernen, er kuglen effektivt indlejret som koncentriske skaller.
P-orbitaler
Når n overstiger én, opstår der yderligere orbitaltyper. For l lig med én kaldes orbitalen en p orbital. Disse ligner håndvægte. Hvert l værdien tillader m til at gå fra –l til +l i heltalstrin, hvilket giver tre p-orbitaler på hvert niveau over n=1:en orienteret langs z-aksen (m=0) og to ortogonale i x-y-planet (m=±1). P-orbitaler vises i alle hovedenerginiveauer over det første, med subtile strukturelle ændringer som n vokser.
D orbitaler
Ved n=3, l kan være 2, hvilket giver anledning til d orbitaler. Der er fem distinkte d-orbitaler svarende til m =–2, –1, 0, 1, 2. m=0 d orbitalen ligner en håndvægt med en ringformet "donut" i midten, mens de andre fire ligner fire lapper arrangeret i en firkantet pyramide, hver orienteret forskelligt. D-orbitaler er til stede, når det primære kvantetal er mindst tre.
F-orbitaler
For n=4, l er lig med 3, hvilket producerer f orbitaler. Disse er de mest komplekse og svære at visualisere. m=0, ±1 orbitaler ligner håndvægte med to ringformede ringe, der flankerer den centrale stang, hvorimod de resterende m-værdier producerer former, der ligner bundter af otte balloner bundet sammen i en central knude. F orbitaler bliver tilgængelige i alle energiniveauer, hvor n er fire eller større.
Visualiseringer
Matematikken bag elektronorbitaler er indviklet, men adskillige onlineværktøjer gengiver disse former grafisk. Sådanne visualiseringer er uvurderlige til at forstå, hvordan elektroner fordeler sig omkring en kerne.
 Varme artikler
Varme artikler
-
 Rapid DNA identificerer ofre for undfangelsesbådbrandKredit:U.S. Department of Homeland Security 34 mennesker døde i en tragisk bådbrand den 2. september. 2019, ud for Santa Cruz Islands kyst, Californien. Fem besætningsmedlemmer slap med skader eft
Rapid DNA identificerer ofre for undfangelsesbådbrandKredit:U.S. Department of Homeland Security 34 mennesker døde i en tragisk bådbrand den 2. september. 2019, ud for Santa Cruz Islands kyst, Californien. Fem besætningsmedlemmer slap med skader eft -
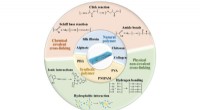 Hydrogel fremmer sårheling bedre end traditionelle bandager, gazebindTværbindingsmekanismer og råmaterialer til forskellige hydrogel sårbandager. Kredit:Zheng Pan, Huijun Ye, og Decheng Wu Den udbredte brug af højhastigheds- og højenergivåben i moderne krigsførelse
Hydrogel fremmer sårheling bedre end traditionelle bandager, gazebindTværbindingsmekanismer og råmaterialer til forskellige hydrogel sårbandager. Kredit:Zheng Pan, Huijun Ye, og Decheng Wu Den udbredte brug af højhastigheds- og højenergivåben i moderne krigsførelse -
 Udvikling af enzymer til at omdanne planteaffald til bæredygtige produkterDet nyudviklede enzym. Kredit:University of Portsmouth En ny familie af enzymer er blevet konstrueret til at udføre et af de vigtigste trin i omdannelsen af planteaffald til bæredygtige og højvæ
Udvikling af enzymer til at omdanne planteaffald til bæredygtige produkterDet nyudviklede enzym. Kredit:University of Portsmouth En ny familie af enzymer er blevet konstrueret til at udføre et af de vigtigste trin i omdannelsen af planteaffald til bæredygtige og højvæ -
 Sådan regenereres aktivt kul:En trin-for-trin guideAf ShamikaM Opdateret 24. marts 2022 Hvad du skal bruge 9-10 % hydrogenperoxidopløsning (håndteres med handsker) Destilleret, deioniseret vand (valgfrit) Aktivt kul er en meget porøs form for kul,
Sådan regenereres aktivt kul:En trin-for-trin guideAf ShamikaM Opdateret 24. marts 2022 Hvad du skal bruge 9-10 % hydrogenperoxidopløsning (håndteres med handsker) Destilleret, deioniseret vand (valgfrit) Aktivt kul er en meget porøs form for kul,
- DIY: At lave en signalstyrkemåler
- At undertrykke kedsomhed på arbejdet skader fremtidig produktivitet, viser undersøgelse
- Det tungeste dyr nogensinde? Forskere opdager massive gamle hvaler
- Vulkanskråninger byder på frodige, overkommeligt stykke paradis
- Når grundstoffer kombineres for at danne forbindelser, ændres deres egenskaber ikke.?
- Hvilke gasser er der i atmosfæren?


