Hvorfor kuldioxid opløses i vand:Videnskaben bag opløselighed og kulsyre
Når du åbner en flaske sodavand, er det brusende brus en visuel påmindelse om kuldioxid (CO2 ) molekyler opløst i vand. Forstå hvorfor CO2 opløses så let involverer en blanding af molekylær polaritet, ligevægtskemi og fysiske principper, der styrer gasopløselighed.
Molekylær polaritet af CO2
CO2 er et lineært molekyle sammensat af et carbonatom dobbeltbundet til to oxygenatomer. Selvom bindingerne er symmetriske, er ilt mere elektronegativt end kulstof, hvilket giver en lille negativ ladning på hver iltende. Denne polaritet skaber en attraktiv interaktion med det polære vand (H2 O) molekyler, hvilket tillader CO2 skal indhylles i en hydreringsskal.
Opløsningsprocessen
For CO2 for at opløses skal det først krydse luft-vand-grænsefladen. Når først de er inde i væsken, bliver gasmolekylerne omgivet af vandmolekyler - en proces styret af Henrys lov. Ved en given temperatur er koncentrationen af opløst CO2 er direkte proportional med dets partialtryk i gasfasen.
Ligevægt med kulsyre
Ikke alt opløst CO2 forbliver som fri gas. En lille fraktion reagerer med vand og danner kulsyre (H2 CO3 ), en ligevægt, der forløber langsomt:\[\text{CO}_{2(g)} + \text{H}_{2}\text{O} \rightleftharpoons \text{H}_{2}\text{CO}_{3}\]Carbonsyre er svag og kan yderligere dissociere til bicarbonat (HCO3 – ) og carbonat (CO3 2– ) ioner, der frigiver hydrogenioner (H + ), der sænker opløsningens pH.
Kulsyre i drikkevarer
Kommercielt kulsyreholdige drikke fremstilles ved at forcere CO2 i vand under højt tryk. Dette øger koncentrationen af opløst gas ud over, hvad ligevægt ved omgivende tryk ville tillade. Kolde temperaturer øger opløseligheden yderligere, hvilket er grunden til, at mousserende vand smager sprødere, når det er afkølet.
Hvorfor sodavand bliver fladt
Når flasken åbnes, falder trykket, og CO2 begynder at undslippe som bobler. Fordi tiltrækningen mellem vand og CO2 er svagere end mellem vand og sukkerarter eller salte, forsvinder gassen lettere, hvilket får drikkevaren til at "flade ud".
Vigtige ting
- CO2 opløses i vand på grund af dens lille polaritet og den resulterende hydreringsskal.
- Henrys lov regulerer mængden af CO2 der kan opløses ved et givet tryk og temperatur.
- En lille del af opløst CO2 danner kulsyre, som dissocierer til bicarbonat- og carbonationer, hvilket gør opløsningen let forsuret.
- Højt tryk og lav temperatur er afgørende for at maksimere kulsyre i drikkevarer.
 Varme artikler
Varme artikler
-
 Forstå Runaway Polymerization:Risici og forebyggelseBrand X Pictures/Brand X Pictures/Getty Images En løbsk polymerisation er en potentielt farlig reaktion, hvor kemiske produkter dannes med for høj hastighed og producerer varme, der kan føre til en
Forstå Runaway Polymerization:Risici og forebyggelseBrand X Pictures/Brand X Pictures/Getty Images En løbsk polymerisation er en potentielt farlig reaktion, hvor kemiske produkter dannes med for høj hastighed og producerer varme, der kan føre til en -
 Verifikation af whisky ved hjælp af laserlysKredit:CC0 Public Domain Forskere fra University of St Andrews har udviklet en innovativ ny teknik ved hjælp af lasere til nøjagtigt at måle ægtheden af nogle af verdens mest eksklusive whiskyer
Verifikation af whisky ved hjælp af laserlysKredit:CC0 Public Domain Forskere fra University of St Andrews har udviklet en innovativ ny teknik ved hjælp af lasere til nøjagtigt at måle ægtheden af nogle af verdens mest eksklusive whiskyer -
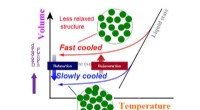 Skræddersyet hærdning af bulk metallisk glas induceret af 2-D gradientforyngelseEn skematisk illustration af metallisk glas med forskellige afslapningstilstande afhængigt af afkølingshastigheden. Kredit:Tohoku University Et team på Tohoku University har perfektioneret en ny v
Skræddersyet hærdning af bulk metallisk glas induceret af 2-D gradientforyngelseEn skematisk illustration af metallisk glas med forskellige afslapningstilstande afhængigt af afkølingshastigheden. Kredit:Tohoku University Et team på Tohoku University har perfektioneret en ny v -
 Forskere foreslog en måde at fremstille vandopløselige fullerenforbindelser til medicinKredit:CC0 Public Domain Forskere fra Skoltech Center for Energividenskab og Teknologi (CEST) og Institute for Problems of Chemical Physics ved det russiske videnskabsakademi har i samarbejde med
Forskere foreslog en måde at fremstille vandopløselige fullerenforbindelser til medicinKredit:CC0 Public Domain Forskere fra Skoltech Center for Energividenskab og Teknologi (CEST) og Institute for Problems of Chemical Physics ved det russiske videnskabsakademi har i samarbejde med


