Hvordan atomer binder sig til dannelse af forbindelser:En klar guide til ioniske, kovalente, metalliske og hydrogenbindinger
Af Carolyn Kaberline | Opdateret 24. marts 2022
Billede udlånt af Prill/iStock/GettyImages
Mens atomer kan eksistere som isolerede enheder, kombinerer de oftest med andre atomer for at skabe forbindelser. Den mindste stabile enhed af en forbindelse kaldes et molekyle, og dets dannelse afhænger af typen af kemisk binding, der holder atomerne sammen. De fire primære bindingstyper - ionisk, kovalent, metallisk og hydrogen - har hver deres særskilte mekanismer og giver unikke egenskaber til de resulterende molekyler.
Ionisk binding
Ionbindinger dannes, når et atom donerer en eller flere valenselektroner til et andet, hvilket skaber modsat ladede ioner, der tiltrækker elektrostatisk. Et klassisk eksempel er natrium (Na), der reagerer med klor (Cl). Natrium, med en enkelt elektron i sin ydre skal, mister let denne elektron og bliver til Na⁺, mens klor, næsten fuld ved syv valenselektroner, får en elektron til at blive Cl⁻. Den elektrostatiske tiltrækning mellem Na⁺ og Cl⁻ resulterer i den neutrale, stabile forbindelse natriumchlorid (NaCl). Ionbinding involverer typisk en fuldstændig overførsel af elektroner og er mest almindelig mellem metaller og ikke-metaller.
Kovalent binding
I modsætning hertil opstår kovalente bindinger, når atomer deler valenselektroner i stedet for at overføre dem. Ikke-metalatomer - såsom kulstof, oxygen og nitrogen - har tendens til at danne kovalente bindinger. Ved at dele elektroner opnår hvert atom en stabil elektronkonfiguration, ofte oktetreglen. Afhængigt af antallet af delte elektronpar kan kovalente bindinger være enkelt (et par), dobbelt (to par) eller tredobbelt (tre par). For eksempel danner et oxygenmolekyle (O₂) en dobbelt kovalent binding mellem to oxygenatomer, mens nitrogen (N2) har en tredobbeltbinding. Disse delte elektroner tillader molekyler at eksistere i en afbalanceret, lavenergitilstand.
Metallisk binding
Metallisk binding forekommer udelukkende blandt metalatomer. I dette arrangement delokaliseres valenselektroner og danner et "hav af elektroner", der bevæger sig frit omkring et gitter af positivt ladede metalioner. Denne elektronmobilitet tegner sig for metallers kendetegn:elektrisk ledningsevne, termisk ledningsevne, duktilitet og formbarhed. For eksempel er kobbers fremragende elektriske ydeevne og jerns evne til at blive hamret til tynde plader direkte konsekvenser af dets metalliske bindingsstruktur.
Brintbinding
Hydrogenbinding er en specialiseret, men alligevel kraftig, intermolekylær kraft, der opstår, når hydrogen, bundet til et meget elektronegativt atom (ilt, nitrogen eller fluor), oplever en delvis positiv ladning. Det elektronegative atom bærer en delvis negativ ladning, hvilket tillader et molekyles brint at tiltrække det negative sted af et andet. Denne polaritet er årsagen til, at vand (H2O) molekyler klæber sammen, hvilket giver vand dets høje overfladespænding og evne til at opløse mange stoffer. Hydrogenbindinger påvirker også strukturen af proteiner og DNA.
Bindingsresultater
Atomer kan indgå i mere end én bindingstype afhængigt af deres partnere. For eksempel kan magnesium (Mg) danne en ionbinding med et ikke-metal som chlor (MgCl₂) eller en metallisk binding med andre magnesiumatomer i et metalgitter. Uanset bindingstypen er slutresultatet en stabil forbindelse med forskellige fysiske og kemiske egenskaber – egenskaber, der understøtter alt fra hverdagsmaterialer til avancerede teknologier.
At forstå disse bindingsmekanismer er grundlæggende for kemi, materialevidenskab og utallige anvendte områder. By grasping how atoms interact, scientists can predict material behavior, design new substances, and innovate across industries.
 Varme artikler
Varme artikler
-
 Videnskaben bag vandfrysning:Fra molekyler til isudvidelseAf Ann Johnson, Opdateret 24. marts 2022 Molekylær bevægelse under frysning Når vand skifter fra flydende til fast stof, går dets molekyler fra en konstant, kaotisk dans til et højt ordnet gitter. I
Videnskaben bag vandfrysning:Fra molekyler til isudvidelseAf Ann Johnson, Opdateret 24. marts 2022 Molekylær bevægelse under frysning Når vand skifter fra flydende til fast stof, går dets molekyler fra en konstant, kaotisk dans til et højt ordnet gitter. I -
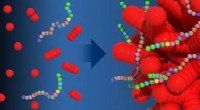 Koralformede nanopartikler bygget af design ved hjælp af konstruerede peptoiderI en ny undersøgelse ledet af PNNL-materialeforsker Chun-Long Chen, sekvensdefinerede peptoider (vist her som kæder af små farverige kugler) muliggjorde den forudsigelige morfologiske udvikling af sfæ
Koralformede nanopartikler bygget af design ved hjælp af konstruerede peptoiderI en ny undersøgelse ledet af PNNL-materialeforsker Chun-Long Chen, sekvensdefinerede peptoider (vist her som kæder af små farverige kugler) muliggjorde den forudsigelige morfologiske udvikling af sfæ -
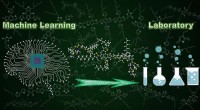 Maskinlæringsassisteret molekylært design til højtydende organiske fotovoltaiske materialerBrug af maskinlæring til at hjælpe molekylært design. Kredit:Wenbo Sun, Videnskabens fremskridt, doi:10.1126/sciadv.aay4275 At syntetisere højtydende materialer til organisk fotovoltaik (OPVer), d
Maskinlæringsassisteret molekylært design til højtydende organiske fotovoltaiske materialerBrug af maskinlæring til at hjælpe molekylært design. Kredit:Wenbo Sun, Videnskabens fremskridt, doi:10.1126/sciadv.aay4275 At syntetisere højtydende materialer til organisk fotovoltaik (OPVer), d -
 Jagten på en bedre solcremeKredit:Pixabay/CC0 Public Domain Mange sommerdage starter med at smøre solcreme på for at forhindre solskoldning, hudskader og hudkræft. En almindelig ingrediens i solcremer er avobenzon, som virke
Jagten på en bedre solcremeKredit:Pixabay/CC0 Public Domain Mange sommerdage starter med at smøre solcreme på for at forhindre solskoldning, hudskader og hudkræft. En almindelig ingrediens i solcremer er avobenzon, som virke
- Hvad er koordinaterne og graderne af Taurus -konstellationen?
- Hvad er bølgelængden af grundlæggende resonansfrekvens et lukket rør 35 cm lang?
- Lever vira de eneste infektiøse agenter?
- En stjerne er født:Ved hjælp af lasere til at undersøge, hvordan stjernemateriale fremstilles
- Sådan konverteres mol til molekyler
- Astronomer opdager ny kemisk signatur i en exoplanetatmosfære ved hjælp af Subaru-teleskopet


