Beregning af pKa af en svag syre:En trin-for-trin guide
Af Mike Gamble | Opdateret 24. marts 2022
En syres pKa kvantificerer dens tendens til at dissociere i vandig opløsning. Mens stærke syrer ioniserer fuldstændigt, er pKa-værdien især nyttig for svage syrer, hvilket muliggør forudsigelser af pH ved kendte koncentrationer og hjælper med syreidentifikation, når forbindelsen er ukendt.
Trin 1 – Bestem hydrogen-ion-koncentrationen
Beregn [H⁺] fra opløsningens pH ved hjælp af forholdet [H⁺] =10 –pH . For eksempel giver en pH på 2,29 [H⁺] =5,13×10⁻³ molL⁻¹ .
Trin 2 – Beregn dissociationskonstanten (Ka)
Brug udtrykket Ka =[H⁺]² / ( [HA] – [H⁺] ) , hvor [HA] er den oprindelige syrekoncentration. Med en startkoncentration på 0,15 molL⁻¹, Ka =(5,13×10⁻³)² / (0,15 – 5,13×10⁻³) =1,82×10⁻⁴ .
Trin 3 – Konverter til pKa
Til sidst opnås pKa via pKa =–log₁₀(Ka) . Ved at bruge Ka ovenfor, pKa =–log₁₀(1,82×10⁻⁴) =3,74 .
Sidste artikelVarier pH nøjagtigt for at måle enzymaktivitet
Næste artikelSølvlodning af rustfrit stål:teknikker, tips og begrænsninger
 Varme artikler
Varme artikler
-
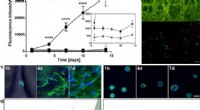 Engineering ECM-lignende fibre med bioaktiv silke til 3-D cellekulturSpredning og udvidelse af celler i FN-silke sammenlignet med når de er indkapslet i en RGD-koblet hydrogel. (a) repræsentativ graf (middelværdi og standardafvigelse) for Alamar Blue-levedygtighedsassa
Engineering ECM-lignende fibre med bioaktiv silke til 3-D cellekulturSpredning og udvidelse af celler i FN-silke sammenlignet med når de er indkapslet i en RGD-koblet hydrogel. (a) repræsentativ graf (middelværdi og standardafvigelse) for Alamar Blue-levedygtighedsassa -
 Forskere forenkler og strømliner organisk kemisk syntese dramatiskFor første gang opdagede forskere en enkel og yderst effektiv måde at fremstille visse former for organiske forbindelser på. Holdet fra Institut for Kemi ved University of Tokyo rapporterer, at deres
Forskere forenkler og strømliner organisk kemisk syntese dramatiskFor første gang opdagede forskere en enkel og yderst effektiv måde at fremstille visse former for organiske forbindelser på. Holdet fra Institut for Kemi ved University of Tokyo rapporterer, at deres -
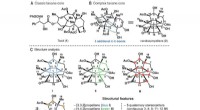 Endelig syntetisk canataxpropellan:Reproducerer et af naturens mest komplekse produkterSammenligning af Taxol-kernen med den komplekse taxankerne og nøgletræk ved (–)-canataxpropellane (2). Kredit: Videnskab (2020). DOI:10.1126/science.aay9173 Et team af kemikere ved universitetet
Endelig syntetisk canataxpropellan:Reproducerer et af naturens mest komplekse produkterSammenligning af Taxol-kernen med den komplekse taxankerne og nøgletræk ved (–)-canataxpropellane (2). Kredit: Videnskab (2020). DOI:10.1126/science.aay9173 Et team af kemikere ved universitetet -
 De miljømæssige omkostninger ved kontaktlinserKontaktlinser genvundet fra behandlet spildevandsslam kan skade miljøet. Kredit:Charles Rolsky Mange mennesker er afhængige af kontaktlinser for at forbedre deres syn. Men disse synskorrigerende e
De miljømæssige omkostninger ved kontaktlinserKontaktlinser genvundet fra behandlet spildevandsslam kan skade miljøet. Kredit:Charles Rolsky Mange mennesker er afhængige af kontaktlinser for at forbedre deres syn. Men disse synskorrigerende e
- Gør begge alleler af et genpar en organismergenotype?
- Landformer, at USA og Canada Share
- Forskere kaster lys over en mere nøjagtig måde at estimere klimaændringer på
- Forskellene mellem Mitokondrier og Kloroplaster i Struktur
- Hvordan ser et kinetisk energibillede ud?
- Bevægelser af solen, månen og jorden


