Beregning af antallet af atomer i enhver prøve:En klar, trin-for-trin guide
Af Rosann Kozlowski
Opdateret 24. marts 2022
Vil du vide, hvor mange atomer der er i en given mængde af et stof? Ved at kombinere nogle få vigtige oplysninger - molær masse, prøvemasse og Avogadros tal - kan du bestemme det nøjagtige atomantal. Denne guide guider dig gennem processen med et praktisk kobbereksempel.
Trin 1:Bestem stoffets molære masse
Se et periodisk system for at finde atommassen af hvert grundstof i din forbindelse. For et rent grundstof som kobber vises atommassen direkte under dets symbol. Kobbers atommasse er 63,55 g/mol , hvilket betyder, at et mol kobberatomer vejer 63,55 gram.
For forbindelser summeres atommasserne af alle indgående atomer. Den resulterende værdi er den molære masse, udtrykt i gram pr. mol.
Trin 2:Konverter prøvemassen til mol
Brug molmassen til at oversætte den kendte masse af din prøve til mol. Beregningen følger et simpelt enhedsannulleringsforhold:
32.80 g Cu × 1 mol Cu / 63.55 g Cu = 0.52 mol Cu
I dette eksempel svarer 32,80 gram kobber til 0,52 mol.
Trin 3:Oversæt muldvarpe til atomer med Avogadros nummer
Avogadros nummer—6.022×10 23 - er antallet af enheder i et mol af ethvert stof. Multiplicer molmængden med denne konstant for at finde atomantallet:
0.52 mol Cu × 6.022 × 1023 atoms/mol = 3.13 × 1023 atoms
Således indeholder 32,80 gram kobber cirka 3,13×10 23 atomer.
Trin 2 og 3 kan kombineres til én linje:
32.80 g Cu × 1 mol Cu / 63.55 g Cu × 6.022 × 1023 atoms/mol = 3.13 × 1023 atoms
Til hurtige beregninger kan du bruge onlineværktøjer såsom Omni-beregneren , selvom du stadig skal kende molmassen for at indtaste korrekt.
Historisk note:Oprindelsen af Avogadros nummer
Avogadros nummer er opkaldt efter den italienske videnskabsmand Amedeo Avogadro (1776-1856), som foreslog, at lige store mængder gasser ved samme temperatur og tryk indeholder lige mange molekyler. Selvom han ikke definerede den nøjagtige værdi på 6.022×10 23 , fik hans grundlæggende arbejde konstanten hans navn. Avogadros teori blev først offentliggjort i 1811 og fik først udbredt accept et halvt århundrede senere.
 Varme artikler
Varme artikler
-
 Biobaseret forbindelse tilbyder et grønnere kulfiberalternativDen her viste katalytiske reaktor er til omdannelse af kemiske mellemprodukter til acrylonitril. Arbejdet er en del af Renewable Carbon fiber Consortium. Kredit:Dennis Schroeder/NREL Fra biler og
Biobaseret forbindelse tilbyder et grønnere kulfiberalternativDen her viste katalytiske reaktor er til omdannelse af kemiske mellemprodukter til acrylonitril. Arbejdet er en del af Renewable Carbon fiber Consortium. Kredit:Dennis Schroeder/NREL Fra biler og -
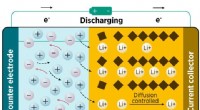 Røntgenanalyse afslører opladningsmekanismen for et lovende elektrodematerialeEn titaniumdioxidelektrode optager lithiumioner, når batteriet aflades. Kredit:Ref. 1. © 2018 Wiley-VCH Verlag GmbH &Co. KGaA, Weinheim En eksperimentel teknik udviklet af A*STAR-forskere er bleve
Røntgenanalyse afslører opladningsmekanismen for et lovende elektrodematerialeEn titaniumdioxidelektrode optager lithiumioner, når batteriet aflades. Kredit:Ref. 1. © 2018 Wiley-VCH Verlag GmbH &Co. KGaA, Weinheim En eksperimentel teknik udviklet af A*STAR-forskere er bleve -
 Fremstilling af metal-organiske ramme-baserede kompositter for effektivitetKandidatstuderende Yufeng Quan og Ruiqing Shen bruger en dobbeltskrueekstruder i bænkskala til bæredygtig og effektiv fremstilling af metal-organiske ramme-baserede polymer nanokompositter. Kredit:Dr.
Fremstilling af metal-organiske ramme-baserede kompositter for effektivitetKandidatstuderende Yufeng Quan og Ruiqing Shen bruger en dobbeltskrueekstruder i bænkskala til bæredygtig og effektiv fremstilling af metal-organiske ramme-baserede polymer nanokompositter. Kredit:Dr. -
 Kunstigt blad som minifabrik til medicinSelv med det blotte øje er mængden af lys fanget af mini-fabrikkerne synlig, lyser knaldrødt. Venerne gennem bladene er de tynde kanaler, som væske kan pumpes igennem. Startprodukterne kommer ind i
Kunstigt blad som minifabrik til medicinSelv med det blotte øje er mængden af lys fanget af mini-fabrikkerne synlig, lyser knaldrødt. Venerne gennem bladene er de tynde kanaler, som væske kan pumpes igennem. Startprodukterne kommer ind i
- Undersøgelse analyserer nøglerne til fragmentering af metalliske materialer
- Hvordan en amerikansk stat gik fra to jordskælv om året til 585
- Når elementer kemisk binder sammen, laver de en?
- Hvad er en one-celle organisme?
- Algoritme identificerer optimale par til at sammensætte metal-organiske rammer
- Lyser vejen til forbedrede biomaterialer


