Konvertering af millimoler til dele pr. million (PPM):En praktisk vejledning
Af Kevin Beck, Opdateret 24. marts 2022
Hvis du kender volumen og molariteten af en opløsning, kan du hurtigt bestemme millimol (mmol) af det tilstedeværende opløste stof. Fra denne værdi kan du konvertere til milligram (mg) og i sidste ende beregne koncentrationen i dele pr. million (PPM).
Forstå PPM
Mens molaritet er udtrykt i mol pr. liter (mol/L), er PPM en masse-per-volumen-metrik. En PPM svarer til et milligram opløst stof i en liter opløsning - i det væsentlige mg/L. Udtrykket afspejler, at nævneren er en million gange tælleren i standardenheder.
Eksempel:500 ml 0,1 M kaliumopløsning
Trin 1:Identificer molarmassen
Den molære masse af kalium (K) er 39,098 g/mol. Således vejer 1 mmol kalium 39,098 mg.
Trin 2:Beregn millimoler i prøven
Volumen =0,5 L (500 ml). Med en koncentration på 0,1 M:\[\tekst{mol} =0,5\tekst{ L} \ gange 0,1\tekst{ mol/L} =0,05\tekst{ mol}\]
Da 1 mol =1.000 mmol, indeholder prøven 50 mmol kalium.
Trin 3:Konverter millimoler til masse
Masse =50 mmol × 39,098 mg/mmol =1.954,9 mg (≈1.955 mg).
Trin 4:Udtryk som PPM
PPM =mg/L. Med 1.955 mg i 0,5 L:\[\text{PPM} =\frac{1.955\text{ mg}}{0,5\text{ L}} =3.910\text{ PPM}\]
Nøgletilbehør
PPM er især nyttigt til at måle spormængder af stoffer - ofte giftige eller miljømæssigt signifikante - inden for en stor mængde opløsningsmiddel. For faste stoffer såsom jord eller gasser omfatter relaterede enheder PPMm (masse pr. masse) og PPMv (volumen pr. volumen).
Ved at følge disse trin kan du pålideligt konvertere millimol til PPM for enhver vandig opløsning.
Sidste artikelHurtigt at finde vandrette asymptoter med en TI-83
Næste artikelLigevægtskonstant (K):Beregning og betydning
 Varme artikler
Varme artikler
-
 Hvordan temperatur driver overgangen mellem fast, flydende og gasAf Matthew Perdue Opdateret 24. marts 2022 showcake/iStock/Getty Images Temperaturen afspejler den gennemsnitlige kinetiske energi af de molekyler, der udgør et stof. Uanset om du måler det i Celsiu
Hvordan temperatur driver overgangen mellem fast, flydende og gasAf Matthew Perdue Opdateret 24. marts 2022 showcake/iStock/Getty Images Temperaturen afspejler den gennemsnitlige kinetiske energi af de molekyler, der udgør et stof. Uanset om du måler det i Celsiu -
 Hvordan molekylestørrelse former væskeviskositetFascinadora/iStock/GettyImages Viskositet kvantificerer en væskes modstand mod strømning. Blandt mange påvirkningsfaktorer spiller størrelsen af dets konstituerende molekyler en central rolle. Når
Hvordan molekylestørrelse former væskeviskositetFascinadora/iStock/GettyImages Viskositet kvantificerer en væskes modstand mod strømning. Blandt mange påvirkningsfaktorer spiller størrelsen af dets konstituerende molekyler en central rolle. Når -
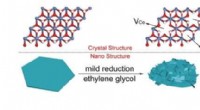 Rige defekter, der øger iltudviklingsreaktionenIllustration af den solvotermiske reaktion af uberørte CoFe LDHer ved at bruge ethylenglycol. Kredit:©Science China Press Iltudviklingsreaktionen (OER) med træg reaktionskinetik og stort overpoten
Rige defekter, der øger iltudviklingsreaktionenIllustration af den solvotermiske reaktion af uberørte CoFe LDHer ved at bruge ethylenglycol. Kredit:©Science China Press Iltudviklingsreaktionen (OER) med træg reaktionskinetik og stort overpoten -
 Video:Kan blanding af husholdningsrengøringsmidler dræbe dig?Kredit:The American Chemical Society Når badeværelset begynder at se grimt ud, og det er tid til at piske gule handsker frem, det eneste, der betyder noget, er at få arbejdet udført hurtigt. Så d
Video:Kan blanding af husholdningsrengøringsmidler dræbe dig?Kredit:The American Chemical Society Når badeværelset begynder at se grimt ud, og det er tid til at piske gule handsker frem, det eneste, der betyder noget, er at få arbejdet udført hurtigt. Så d
- Undersøgelse bekræfter indflydelsen af planetariske tidevandskræfter på solaktivitet
- Yellowstone National Park er varmere end nogensinde
- I en æra med Brexit og falske nyheder, forskere skal omfavne sociale medier
- Ultra-hvid belægning modelleret på bille-skæl
- Forskere viser, at heparansulfat justerer funktionerne af vækstfaktorproteiner
- Hvad parrer adenin i RNA?


