Forståelse af fast koncentration:definitioner og beregninger
Af Jack Brubaker Opdateret 24. marts 2022
Uanset om en blanding indeholder to blandede faste stoffer, to blandede væsker eller et fast stof opløst i en væske, kaldes forbindelsen til stede i den største mængde "opløsningsmidlet", og forbindelsen til stede i den mindre mængde kaldes "opløst stof". I en fast/fast blanding udtrykkes koncentrationen af opløst stof lettest som masseprocent. Hvis det opløste stof er ekstremt fortyndet (dvs. væsentligt mindre end 1 vægtprocent), så udtrykkes koncentrationen sædvanligvis som dele pr. million (ppm). Nogle beregninger, der involverer koncentration, kræver, at det opløste stof udtrykkes som en molfraktion.
Trin 1
Beregn koncentrationen i masseprocent ved at dividere massen af det opløste stof med prøvens samlede masse og gange med 100. For eksempel, hvis en prøve af en metallegering indeholder 26 g nikkel (Ni), og prøvens samlede masse er 39 g, så
(26 g Ni) / (39 g) x 100 =67 % Ni
Trin 2
Udtryk koncentrationen af fortyndede opløste stoffer i ppm ved at dividere massen af det opløste stof med prøvens samlede masse og gange med 1.000.000. Således, hvis en prøve af metallegering kun indeholder 0,06 g Ni, og prøvens samlede masse er 105 g, så
(0,06 g Ni) / (105 g) x 1.000.000 =571 ppm
Trin 3
Beregn molfraktion ved at dividere mol opløst stof med det samlede antal mol opløst stof og opløsningsmiddel. Dette involverer først at omdanne masserne af det opløste stof og opløsningsmidlet til mol, hvilket kræver viden om mængderne af både opløst stof og opløsningsmiddel. Omdannelsen til mol kræver yderligere formelvægtene af det opløste stof og opløsningsmidlet. Overvej for eksempel en nikkel/jern (Ni/Fe) legering, der indeholder 25 g Ni og 36 g Fe. Formelvægten af Ni (bestemt ud fra det periodiske system) er 58,69 gram pr. mol (g/mol), og formelvægten af Fe er 55,85 g/mol. Derfor,
Mol Ni =(25 g) / (58,69 g/mol) =0,43 mol
Mol Fe =(36 g) / (55,85) =0,64 mol
Molfraktionen af Ni er så givet ved (0,43) / (0,43 + 0,64) =0,40.
 Varme artikler
Varme artikler
-
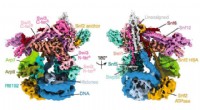 Forskere kortlægger strukturen af det centrale kromatin-ombygningskompleksKredit:Northwestern University Northwestern University-forskere har kortlagt en gruppe proteiner, der spiller en afgørende rolle i både genekspression og reparation af beskadiget DNA. Ved at forst
Forskere kortlægger strukturen af det centrale kromatin-ombygningskompleksKredit:Northwestern University Northwestern University-forskere har kortlagt en gruppe proteiner, der spiller en afgørende rolle i både genekspression og reparation af beskadiget DNA. Ved at forst -
 Krypteret, one-touch, menneske-maskine interface-teknologi afslører brugerfysiologiSikker og ikke-invasiv fingeraftryksbiosensor kan detektere molekyler, der cirkulerer i kroppen. Kredit:UCLA/Interconnected &Integrated Bioelectronics Lab Forskere ved UCLA og Stanford University h
Krypteret, one-touch, menneske-maskine interface-teknologi afslører brugerfysiologiSikker og ikke-invasiv fingeraftryksbiosensor kan detektere molekyler, der cirkulerer i kroppen. Kredit:UCLA/Interconnected &Integrated Bioelectronics Lab Forskere ved UCLA og Stanford University h -
 Tager ansvaret:Forskere går sammen om at lave bedre batterierAdjunkt Jose Mendoza-Cortes og postdoc-forsker A. Nijamudheen gik sammen med forskere fra Cornell for at designe et mere effektivt batteri. Kredit:Florida State University Et forskningshold fra Fl
Tager ansvaret:Forskere går sammen om at lave bedre batterierAdjunkt Jose Mendoza-Cortes og postdoc-forsker A. Nijamudheen gik sammen med forskere fra Cornell for at designe et mere effektivt batteri. Kredit:Florida State University Et forskningshold fra Fl -
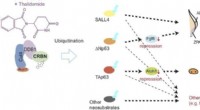 Molekylær basis for lægemiddelvirkninger på lemmer og øreudvikling afsløretThalidomid binder sig til cereblon (CRBN) og forårsager unormal lem- og øreudvikling ved at fremkalde nedbrydning af proteiner kaldet? Np63α og TAp63α gennem en proces kendt som ubiquitination. Denne
Molekylær basis for lægemiddelvirkninger på lemmer og øreudvikling afsløretThalidomid binder sig til cereblon (CRBN) og forårsager unormal lem- og øreudvikling ved at fremkalde nedbrydning af proteiner kaldet? Np63α og TAp63α gennem en proces kendt som ubiquitination. Denne
- Hvad er temperaturen på laboratorietermometre?
- Hvordan skaber blanding varme?
- Hvad er den type opløsning, der er dannet af Creek Water efter kraftigt regn kaldet?
- Mælkevejen Galaxy er medlem af?
- Kviksølv er et metal med smeltepunkt på -39cc og kogende 357cc Hvad staten ved?
- Nano- og mikromotorer til biologiske og kemiske anvendelser


