Beregning af procentvis dissociation af svage syrer – en praktisk vejledning
Når en stærk syre tilsættes vand, dissocieres den fuldstændigt:HA → H + + A - . I modsætning hertil dissocierer svage syrer kun delvist.
Graden af dissociation kvantificeres af syredissociationskonstanten, Ka :
Ka =([H + ][A - ]) / [HA]
hvor parenteserne angiver molære koncentrationer.
Ka er afgørende for at bestemme procenten af en svag syre, der er dissocieret ved en given pH.
Forbinder Ka, pKa og pH
pH er defineret som den negative logaritme (base10) af protonkoncentrationen:
pH =–log10 [H + ] ⇒ [H + ] =10 –pH
Tilsvarende er forholdet mellem Ka og dets logaritmiske modstykke, pKa,:
pKa =–log10 Ka ⇒ Ka =10 –pKa
Med både pKa og pH kendt, kan den procentvise dissociation beregnes direkte.
Eksempel på dissociationsberegning
Overvej en svag syre-HA med en pKa på 4,756. I en opløsning, hvis pH er 3,85, bestemmes procentdelen af HA, der er dissocieret.
- Konverter pKa til Ka og pH til [H
+
]:
- Ka =10 –4,756 =1.754 × 10 –5 M
- [H + ] =10 –3,85 =1.413 × 10 –4 M
- Fordi syren er svag, [H
+
] ≈ [A
-
]. Indsæt disse værdier i Ka-udtrykket:
Ka = ([H+][A−]) / [HA] = (1.413 × 10–4 M)(1.413 × 10–4 M) / [HA]
Løsning for [HA] giver 0,0011375M. - Procent dissociation =([H + ] / [HA]) × 100 % =(1,413 × 10 –4 M / 0,0011375 M) × 100 % =12,42 %.
Fotokredit:stevanovicigor/iStock/GettyImages
 Varme artikler
Varme artikler
-
 Sådan tilberedes en bromthymol blå pH-indikatoropløsningAf Kevin Krause, Opdateret 24. marts 2022 Bromthymolblåt er en meget brugt pH-indikator, der skifter fra gul i sure opløsninger til blå i basiske miljøer. Denne trin-for-trin guide viser, hvordan man
Sådan tilberedes en bromthymol blå pH-indikatoropløsningAf Kevin Krause, Opdateret 24. marts 2022 Bromthymolblåt er en meget brugt pH-indikator, der skifter fra gul i sure opløsninger til blå i basiske miljøer. Denne trin-for-trin guide viser, hvordan man -
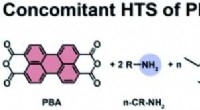 Teamet bruger varmt vand til at danne fotokatalysatorSyntese af n-alkyl-PBI i nærvær af TEOS (n =1, 5, 10 og 100 ækv.). R =n-propylamin (C3), n-pentylamin (C5), n-octylamin (C8), n-tetradecylamin (C14). Kredit:Hipassia M. Moura et al., Journal of Materi
Teamet bruger varmt vand til at danne fotokatalysatorSyntese af n-alkyl-PBI i nærvær af TEOS (n =1, 5, 10 og 100 ækv.). R =n-propylamin (C3), n-pentylamin (C5), n-octylamin (C8), n-tetradecylamin (C14). Kredit:Hipassia M. Moura et al., Journal of Materi -
 Fra bronzealderen til maddåser, her er hvordan tin ændrede menneskehedenTin kommer fra malmen cassiterit. Kredit:Shutterstock/PYP Nævn tin, og de fleste mennesker ville tænke på den typiske blikdåse, bruges til at konservere fødevarer, du opbevarer i dine skabe. Tin b
Fra bronzealderen til maddåser, her er hvordan tin ændrede menneskehedenTin kommer fra malmen cassiterit. Kredit:Shutterstock/PYP Nævn tin, og de fleste mennesker ville tænke på den typiske blikdåse, bruges til at konservere fødevarer, du opbevarer i dine skabe. Tin b -
 Ikke-invasiv mikroskopi detekterer aktiveringstilstand og skelner mellem celletyperMetoder til at udtrække funktioner fra mærkefri immuncelleanalyse. Multivariat etiketfri data, sammensat af både morfologiske og spektrale parametre, bruges til at identificere funktioner på højt nive
Ikke-invasiv mikroskopi detekterer aktiveringstilstand og skelner mellem celletyperMetoder til at udtrække funktioner fra mærkefri immuncelleanalyse. Multivariat etiketfri data, sammensat af både morfologiske og spektrale parametre, bruges til at identificere funktioner på højt nive
- Hvilken type energi kommer direkte fra solen?
- Hvordan får Monera deres mad og energi?
- Når Trebuchet -modvægt heises af soldater, hvilken form for energi, der overføres til maskinen so…
- Google Maps AR-navigation vil hjælpe byens fodgængere
- Ny undersøgelse viser, hvordan myrkolonier opfører sig forskelligt i forskellige miljøer
- Delfiner bruger signaturfløjter til at repræsentere andre delfiner, på samme måde som mennesker …


