Trin-for-trin guide til fremstilling af en steril natriumchloridopløsning
Af Chris Deziel , Opdateret marts242022
Mikumi/iStock/GettyImages
En natriumchloridopløsning (NaCl), almindeligvis kendt som saltvand, er essentiel til mange medicinske, dental- og laboratorieapplikationer. Den mest udbredte koncentration – 0,9 % w/v – er isotonisk med menneskelige kropsvæsker, hvilket gør den ideel til mundskylning, øjenskylning og intravenøs behandling, når den er tilberedt under korrekte sterile forhold.
Blanding af en vægtprocent (isotonisk) løsning
Trin 1 – Klargør vandet
Fyld en ren målekolbe med ca. 80 % af det endelige volumen med destilleret eller sterilt vand. For at lave 100 ml opløsning, hæld 80 ml i kolben.
Trin 2 – Beregn saltmassen
For en 0,9 % (vægt/volumen) isotonisk opløsning skal du veje 9 g ikke-jodiseret bordsalt for hver 100 ml vand. Hvis du har brug for en større volumen, skaler du massen proportionalt (f.eks. 2,9 spsk for en pint).
Trin 3 – Opløs og juster lydstyrken
Tilsæt det målte salt til vandet og hvirv forsigtigt rundt, indtil det er helt opløst. Fyld derefter kolben op med destilleret vand, indtil det endelige ønskede volumen er nået.
Blanding af en molær opløsning til laboratoriearbejde
Trin 1 – Bestem den ønskede molaritet
Forbered en 1-L opløsning ved at beregne den nødvendige masse af NaCl baseret på dens molære masse på 58,44 gmol⁻¹.
Trin 2 – Vej saltet
For 1M, vej 58,44g; for 0,1 M, vej 5,84 g; for 2M, vejer 116,88g, og så videre.
Trin 3 – Opløs i 0,8 L vand
Anbring 0,8 l destilleret vand i en kolbe, tilsæt det beregnede NaCl og ryst, indtil saltet er helt opløst.
Trin 4 – Bring til 1L
Efter opløsning tilsættes yderligere destilleret vand, indtil det samlede volumen når nøjagtigt 1L.
Væsentligt udstyr
- Målekolbe
- Destilleret eller sterilt vand
- Analytisk balance
- Bordsalt (ikke-joderet)
Hurtig oversigt
For en isotonisk mundskylning, kog først destilleret vand, og tilsæt derefter 0,9 % (w/v) ikke-jodiseret salt. Undgå hav- eller stensalt, som kan indføre urenheder.
Sikkerhedsmeddelelse
Hjemmelavede saltvandsopløsninger mangler steriliteten af laboratoriefremstillede opløsninger og bør ikke bruges til iblødsætning af kontaktlinser eller øjenskylning. Til medicinske formål, brug kommercielt fremstillet sterilt saltvand eller tilbered under aseptiske forhold.
 Varme artikler
Varme artikler
-
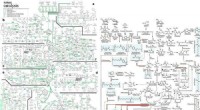 Et omfattende metabolisk kort til produktion af biobaserede kemikalierBiobaseret kemikalieproduktion ad biologiske og kemiske veje. Dette metaboliske kort beskriver repræsentative kemikalier, der kan fremstilles enten ved biologiske og/eller kemiske midler. Røde pile re
Et omfattende metabolisk kort til produktion af biobaserede kemikalierBiobaseret kemikalieproduktion ad biologiske og kemiske veje. Dette metaboliske kort beskriver repræsentative kemikalier, der kan fremstilles enten ved biologiske og/eller kemiske midler. Røde pile re -
 Din næste træstol kunne ankomme flad og derefter tørre til en 3D-formTræblæk trykt som et fladt rektangel er programmeret til at danne en kompleks form efter tørring og størkning. (Lineal er markeret i centimeter.). Kredit:Doron Kam Trægenstande fremstilles normalt
Din næste træstol kunne ankomme flad og derefter tørre til en 3D-formTræblæk trykt som et fladt rektangel er programmeret til at danne en kompleks form efter tørring og størkning. (Lineal er markeret i centimeter.). Kredit:Doron Kam Trægenstande fremstilles normalt -
 Forskerhold øger klæbeevnen af silikone ved at bruge eksemplet med billerForskellige konfigurationer ændrer den klæbende effekt af silikonematerialet, hvis overflade har fået en svampelignende struktur. Vedhæftningen er bedst, når den er bøjet konkav (højre). Kredit:© Emre
Forskerhold øger klæbeevnen af silikone ved at bruge eksemplet med billerForskellige konfigurationer ændrer den klæbende effekt af silikonematerialet, hvis overflade har fået en svampelignende struktur. Vedhæftningen er bedst, når den er bøjet konkav (højre). Kredit:© Emre -
 Forskere til at skabe galaktiske byggesten til at studere rummet mellem stjernerForskere planlægger at syntetisere en klasse af kemiske forbindelser for at afgøre, om de er en vigtig byggesten til fremstilling af galakser. Holdet fra Imperial College London har modtaget startfin
Forskere til at skabe galaktiske byggesten til at studere rummet mellem stjernerForskere planlægger at syntetisere en klasse af kemiske forbindelser for at afgøre, om de er en vigtig byggesten til fremstilling af galakser. Holdet fra Imperial College London har modtaget startfin


