Hvad er osmolaritet? En praktisk guide til osmotisk koncentration
MangoStar_Studio/iStock/GettyImages
Inden for kemi hjælper en række specialiserede enheder videnskabsmænd med at beskrive stoffers egenskaber. Mens pH-skalaen er velkendt til at måle surhedsgrad, er en anden væsentlig enhed - især i medicin - osmolaritet, også kaldet osmotisk koncentration. Osmolaritet kvantificerer mængden af opløst stof, udtrykt i osmol, til stede i et givet volumen opløsning.
TL;DR
Osmolaritet er lig med antallet af osmol opløst stof pr. liter opløsning.
Osmotisk koncentration forklaret
En opløsnings osmolaritet er koncentrationen af dets opløste stof målt i osmol pr. liter (Osm/L). Det afspejler, hvor mange osmoler der er tilgængelige for at påvirke opløsningens osmotiske tryk. Et højere opløsningsmiddelvolumen fortynder det opløste stof, hvilket sænker osmolariteten; omvendt hæver mindre opløsningsmiddel det.
Hvad er en osmole?
En osmol er en ikke-SI-enhed, der repræsenterer antallet af mol opløst stof, der bidrager til en opløsnings osmotiske tryk. Fordi osmoler er specifikt bundet til osmotiske fænomener, bruges de, når trykeffekter betyder noget. I sammenhænge, hvor osmotisk tryk er irrelevant, er millimol per liter (mmol/L) ofte tilstrækkeligt.
Osmotisk tryk i kontekst
Osmotisk tryk er den kraft, der kræves for at standse opløsningsmidlets nettobevægelse over en semipermeabel membran. Osmolaritet informerer direkte om dette tryk:Efterhånden som osmolerne stiger, øges det osmotiske tryk, hvilket driver ligevægten.
Osmolaritet vs. osmolalitet
Mens begge metrikker omhandler koncentration af opløste stoffer, adskiller de sig i referencegrundlag. Osmolaritet måler osmol pr. liter opløsning (Osm/L), hvorimod osmolalitet kvantificerer osmol pr. kilogram opløsningsmiddel (Osm/kg). Valget afhænger af, om volumen eller masse er den mere pålidelige konstant i en given situation.
Sidste artikelFra græsk ild til dynamit:Udviklingen af eksplosive teknologier
Næste artikelNøglekarakteristika for destillerispildevand
 Varme artikler
Varme artikler
-
 Forbedring af varmegenanvendelse med termodiffusionseffektenKredit:CC0 Public Domain Absorptionsvarme transformatorer kan effektivt genbruge spildvarmen, der genereres i forskellige industrier. I disse enheder, specialiserede væsker danner tynde film, når
Forbedring af varmegenanvendelse med termodiffusionseffektenKredit:CC0 Public Domain Absorptionsvarme transformatorer kan effektivt genbruge spildvarmen, der genereres i forskellige industrier. I disse enheder, specialiserede væsker danner tynde film, når -
 Dekontaminering af industrielt plastikaffald for at lette planeternes byrdeKredit:Sofi_Design, Shutterstock Med Europas ambitiøse strategi for plastgenbrug og voksende offentlig bevidsthed, en plastikforureningsfri fremtid synes mere og mere mulig på trods af nuværende f
Dekontaminering af industrielt plastikaffald for at lette planeternes byrdeKredit:Sofi_Design, Shutterstock Med Europas ambitiøse strategi for plastgenbrug og voksende offentlig bevidsthed, en plastikforureningsfri fremtid synes mere og mere mulig på trods af nuværende f -
 Hvad havagurker kan lære os om selvforsvarSej som en havagurk - nyt bevis på, hvordan havagurker producerer selvforsvarskemikalier, kan føre til medicin og sunde forbindelser. Kredit:Frithjof Kuepper University of Aberdeen Genom minedrifts
Hvad havagurker kan lære os om selvforsvarSej som en havagurk - nyt bevis på, hvordan havagurker producerer selvforsvarskemikalier, kan føre til medicin og sunde forbindelser. Kredit:Frithjof Kuepper University of Aberdeen Genom minedrifts -
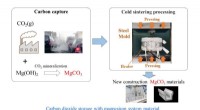 Efterligning af jordskorpen:Undersøgelse af størkning af byggematerialekandidater ved koldsintringCSPen emulerer den sedimentære stendannelsesproces i jordskorpen og letter størkningen af basisk magnesiumcarbonat og hydroxidpulver. Det kan bruges som en metode til at opfange og opbevare kuldioxi
Efterligning af jordskorpen:Undersøgelse af størkning af byggematerialekandidater ved koldsintringCSPen emulerer den sedimentære stendannelsesproces i jordskorpen og letter størkningen af basisk magnesiumcarbonat og hydroxidpulver. Det kan bruges som en metode til at opfange og opbevare kuldioxi


