Opløsning af calciumoxalat med EDTA:En praktisk laboratorievejledning
Af John Brennan Opdateret 24. marts 2022
Calciumoxalat er en ionisk forbindelse med den kemiske formel CaC2O4 og et salt af oxalsyre. Det er meget uopløseligt og opløses dårligt i vand. En metode til at opløse calciumoxalat i laboratoriet er anvendelsen af en forbindelse kaldet ethylendiamintetraeddikesyre eller EDTA. EDTA er yderst effektiv til at binde calciumionerne og derved mindske koncentrationen af calcium i opløsning, hvilket ændrer reaktionsligevægten, så mere calciumoxalat vil opløses. I den procedure, der er skitseret nedenfor, skal du først lave calciumoxalat ved hjælp af almindelige kemikalier og derefter opløse det ved hjælp af EDTA.
Trin 1
Tag beskyttelsesbriller og handsker på. Oxalsyre og calciumoxalat er potentielt giftige, hvis de indtages. Udfør dette eksperiment under stinkskabet for en sikkerheds skyld.
Trin 2
Mål 0,032 ounce (0,9 gram eller ca. 0,01 mol) oxalsyre i bægerglasset og tilsæt lige under 0,338 flydende ounce (10 milliliter) vand. Rør det forsigtigt i bægerglasset, indtil oxalsyren er opløst.
Trin 3
Tilsæt 0,049 ounce (ca. 1,3 gram) calciumchlorid til opløsningen og hvirvl forsigtigt rundt. Efterhånden som reaktionen skrider frem, vil fast calciumoxalat dannes og udfældes fra opløsningen. Du har nu calciumoxalat – det samme stof, som nyresten ofte dannes af.
Trin 4
Tilsæt omkring 0,01 ounce (0,29 gram) EDTA til opløsningen, og hvirvl den forsigtigt i bægerglasset. Noget af calciumoxalatet skulle begynde at opløses.
Ting påkrævet
- EDTA (tilgængelig fra nogle videnskabsbutikker)
- Calciumchlorid (tilgængelig i nogle bil- og isenkræmmerforretninger)
- Oxalsyre (fås i mange byggemarkeder)
- Vand
- Stinkskab
- Sikkerhedsbriller
- Hansker
- Bægerglas
- Måleskala
TL;DR (for lang; læste ikke)
Opløsning af calciumoxalat med EDTA er en anvendelse af Le Chateliers princip. Når calciumoxalat opløses, dissocieres det i calciumioner og oxalationer. Ved at binde calciumionerne med EDTA reducerer vi koncentrationen af produkterne, så vi flytter processen til højre, selvom ligevægtskonstanten ikke ændrer sig. Andre stoffer, der binder eller reagerer med oxalat-ionerne eller calciumionerne, bør også have samme effekt.
Advarsel
Calciumoxalat og oxalsyre er farlige, hvis de indtages eller får lov at komme i kontakt med øjne eller hud. Udfør aldrig dette eksperiment uden handsker, sikkerhedsbriller og korrekt sikkerhedsudstyr. Spis eller drik aldrig præparater af oxalsyre eller calciumoxalat. Indtag aldrig EDTA eller bring det i kontakt med dine øjne eller hud, undtagen som anvist af en læge.
 Varme artikler
Varme artikler
-
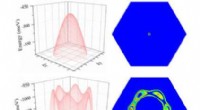 Kunne et nyt 2-D-materiale tillade, at halvledere bliver ved med at blive mindre, stærkere bedre og…I modsætning til andre materialer med elektroner, der spredes i mange retninger (nederst til venstre), elektronerne i 2D -antimon (øverst til venstre) kan fås til at bevæge sig sammen på en ordnet måd
Kunne et nyt 2-D-materiale tillade, at halvledere bliver ved med at blive mindre, stærkere bedre og…I modsætning til andre materialer med elektroner, der spredes i mange retninger (nederst til venstre), elektronerne i 2D -antimon (øverst til venstre) kan fås til at bevæge sig sammen på en ordnet måd -
 Faseovergange fører til nye avancerede materialerKredit:Pixabay/CC0 Public Domain Tro det eller ej, Stål har noget til fælles med bakterielle vedhæng:de kan begge gennemgå en særlig form for fysisk transformation, der forbliver forvirrende. Nu,
Faseovergange fører til nye avancerede materialerKredit:Pixabay/CC0 Public Domain Tro det eller ej, Stål har noget til fælles med bakterielle vedhæng:de kan begge gennemgå en særlig form for fysisk transformation, der forbliver forvirrende. Nu, -
 Forskere producerer de første open source-all-atom-modeller af COVID-19 spike proteinEn model af et S-protein. Kredit:Dr. Yeolkyo Choi/Lehigh Virus SARS coronavirus 2 (SARS-CoV-2) er den kendte årsag til coronavirus sygdom 2019 (COVID-19). Spike- eller S-proteinet letter viral ind
Forskere producerer de første open source-all-atom-modeller af COVID-19 spike proteinEn model af et S-protein. Kredit:Dr. Yeolkyo Choi/Lehigh Virus SARS coronavirus 2 (SARS-CoV-2) er den kendte årsag til coronavirus sygdom 2019 (COVID-19). Spike- eller S-proteinet letter viral ind -
 Opfindelsen af gelé kan helbrede sig selv som menneskelig hudDr. Zhen Jiang og lektor Luke Connal. Kredit:ANU Forskere fra The Australian National University (ANU) har opfundet et nyt gelémateriale, der efterligner biologisk materiale såsom hud, ledbånd og
Opfindelsen af gelé kan helbrede sig selv som menneskelig hudDr. Zhen Jiang og lektor Luke Connal. Kredit:ANU Forskere fra The Australian National University (ANU) har opfundet et nyt gelémateriale, der efterligner biologisk materiale såsom hud, ledbånd og
- Kemisk eller fysisk forandring? Forståelse af naturgasforbrænding
- Hvordan beskriver to måder, hvorpå udviklingen af organismer kan have en skadelig effekt på menne…
- Hvad er de almindelige oxidformler fra Fermium?
- Hvis du har G6PD -mangel, vil fava -bønner ødelægge dine blodlegemer, men det får mindre sandsyn…
- Hvordan er en organisme organiseret lille til stor?
- Kongressen sprænger Boeings fejltrin, FAA fejler MAX, opfordrer til reform


