Bestemmelse af sammensatte polaritet:En trin-for-trin guide
Af Scott Nelson Opdateret 24. marts 2022
En forbindelses polaritet opstår fra den ulige deling af elektroner mellem dets atomer. Når et atom udøver en stærkere elektrontrækkende kraft - dets elektronegativitet - end dets partner, udvikles et dipolmoment, der gør molekylet polært. Derudover påvirker det rumlige arrangement eller symmetrien af atomer polariteten. Typisk bruger kemikere Lewis-punkt- eller valensbindingsdiagrammer til at visualisere elektronfordeling og vurdere polaritet.
Trin 1
Skitser Lewis-strukturen baseret på valenselektronerne for hvert atom.
Trin 2
Identificer ensomme par og anvend VSEPR-modellen til at forudsige molekylets geometri.
Trin 3
Se det periodiske system for at tildele elektronegativitetsværdier til hvert atom, og udregn derefter de relative forskelle på tværs af bindinger.
Trin 4
Evaluer bindingskarakteren - hydrogenbinding, ionisk eller kovalent - for at forstå, hvordan den påvirker ladningsfordelingen.
Trin 5
Bestem den samlede dipol ved at tilføje vektorbidrag af individuelle bindingsmomenter eller ved at bemærke, at symmetriske arrangementer udligner og efterlader et ikke-polært molekyle.
TL;DR
Symmetri afslører ofte polaritet med et blik. Lineære molekyler er typisk ikke-polære, mens bøjede molekyler som vand udviser stærk polaritet.
 Varme artikler
Varme artikler
-
 Biokemikere dykker ned i sundhedsmæssige fordele ved oliven og olivenolieOlivenolie hældes over mad. Kredit:Centers for Disease Control and Prevention. Sundhedsmæssige fordele ved oliven - og tilhørende naturprodukter som olivenolie - er længe blevet anerkendt og udråb
Biokemikere dykker ned i sundhedsmæssige fordele ved oliven og olivenolieOlivenolie hældes over mad. Kredit:Centers for Disease Control and Prevention. Sundhedsmæssige fordele ved oliven - og tilhørende naturprodukter som olivenolie - er længe blevet anerkendt og udråb -
 Forbedring af fraktioneret destillation:Gennemprøvede teknikker for højere renhedAf Sean Lancaster Opdateret 24. marts 2022 Fraktioneret destillation er en hjørnestensteknik til at adskille rene forbindelser fra komplekse blandinger ved at udnytte forskelle i kogepunkter. Ved om
Forbedring af fraktioneret destillation:Gennemprøvede teknikker for højere renhedAf Sean Lancaster Opdateret 24. marts 2022 Fraktioneret destillation er en hjørnestensteknik til at adskille rene forbindelser fra komplekse blandinger ved at udnytte forskelle i kogepunkter. Ved om -
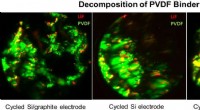 Mod omkostningseffektive løsninger til næste generations forbrugerelektronik, elbiler og elnetNedbrydningen af et polyvinylidenfluorid (PVDF) bindemiddel i et højenergibatteri. Kredit:Jigang Zhou Jagten på et bedre lithium-ion-batteri - et, der kunne holde en mobiltelefon i gang i dagevi
Mod omkostningseffektive løsninger til næste generations forbrugerelektronik, elbiler og elnetNedbrydningen af et polyvinylidenfluorid (PVDF) bindemiddel i et højenergibatteri. Kredit:Jigang Zhou Jagten på et bedre lithium-ion-batteri - et, der kunne holde en mobiltelefon i gang i dagevi -
 Ny klasse af solceller, brug af blyfri perovskitmaterialerBlyfri Perovskite flim (til venstre) og farvefølsomme organiske solceller (højre). Kredit:UNIST Blybaserede perovskiter er lovende materialer til billige og højeffektive solceller. Imidlertid, den
Ny klasse af solceller, brug af blyfri perovskitmaterialerBlyfri Perovskite flim (til venstre) og farvefølsomme organiske solceller (højre). Kredit:UNIST Blybaserede perovskiter er lovende materialer til billige og højeffektive solceller. Imidlertid, den
- Hvad fortæller et spalter dræningsmønster om klipperne under det?
- Er Alaskas første nye sommerfugleart i årtier en gammel hybrid?
- Hvordan bruges solenergi til at generere energi?
- Aluminium reagerer med fortyndet svovlsyre for at producere aluminiumsulfat og brint?
- Forskere finder sikkerhedsforanstaltninger for kvantekommunikation
- En skjult elektronisk overgang S0 til Tn i tung-atomholdige molekyler


