Elementer, der mangler stabile elektronkonfigurationer:en oversigt
Jupiterimages/Photos.com/Getty Images
Et atom består af en kerne indeholdende positivt ladede partikler omgivet af en sky af negativt ladede elektroner. Elektroner i atomer sidder i en række "skaller" rundt om kernen, og hver skal kan indeholde et fast antal elektroner. Grundstoffer, der har en fuld ydre skal, siges at have en stabil elektronkonfiguration. Grundstoffer med stabile elektronkonfigurationer forekommer kun inden for en enkelt kolonne (gruppe 8) i det periodiske system. Derfor har langt størstedelen af grundstofferne i det periodiske system ustabile elektronkonfigurationer.
Brint
Brint
Brint er det enkleste grundstof i det periodiske system og består af en enkelt proton og en enkelt elektron. Den enkelte elektron er placeret i 1s-skallen, som kan besidde to elektroner. Den elektroniske brintkonfiguration er derfor ikke stabil. For at fylde 1s-skallen kombineres to hydrogenatomer og deler den anden elektron. Dette er kendt som kovalent binding og fører i dette tilfælde til dannelsen af et brintmolekyle.
Natrium
Natrium
Natrium er i gruppe 1 i det periodiske system, og hvert atom indeholder 11 elektroner. En enkelt elektron er placeret i den ydre 3s skal, som er i stand til at holde 2 elektroner. Da dette er en ustabil elektronkonfiguration, mister natrium ofte sin ydre 3s elektron, hvilket producerer en positivt ladet ion. Positivt og negativt ladede ioner kombineres for at danne molekyler. Dette er kendt som en ionbinding og fører i natrium til en række forskellige molekyler, herunder natriumchlorid.
Kulstof
Kulstof
Kulstof er i gruppe 6 i det periodiske system og har seks elektroner i alt. Den ydre 2p elektronskal er optaget af to elektroner. Da 2p-skaller kan indeholde seks elektroner, er kulstof ikke i en stabil elektronkonfiguration. For at kulstof kan opnå en stabil elektronkonfiguration, skal det dele yderligere fire elektroner via kovalente bindinger. Det er denne proces, der fører til den store mængde kulstofforbindelser, såsom metan.
Klor
Klor
Klor er i gruppe 7 i det periodiske system og har 17 elektroner. Den ydre 3p-skal er optaget af fem elektroner og kræver derfor en elektron mere for at have en stabil konfiguration. Klor får ofte denne ekstra elektron på bekostning af at blive en negativt ladet ion. Dette betyder, at klor kan kombineres med enhver positivt ladet ion og danne en ionbinding. Et godt eksempel er natriumchlorid, som også er kendt som bordsalt.
 Varme artikler
Varme artikler
-
 Tværfagligt samarbejde giver sværest, tyndeste belægninger endnu opdagetLehigh University-forskerne Nicholas Strandwitz (til venstre) og Brandon Krick (til højre) mener, at de har opdaget det sværeste, tyndeste, mest slidstærke belægninger endnu - plasma-forstærket atomla
Tværfagligt samarbejde giver sværest, tyndeste belægninger endnu opdagetLehigh University-forskerne Nicholas Strandwitz (til venstre) og Brandon Krick (til højre) mener, at de har opdaget det sværeste, tyndeste, mest slidstærke belægninger endnu - plasma-forstærket atomla -
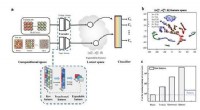 Krystalstruktur forudsigelse af multi-elementer tilfældig legeringKredit:Pohang University of Science &Technology (POSTECH) Alkymi, som forsøgte at gøre billige metaller som bly og kobber til guld, endnu ikke er lykkedes. Imidlertid, med udviklingen af legerin
Krystalstruktur forudsigelse af multi-elementer tilfældig legeringKredit:Pohang University of Science &Technology (POSTECH) Alkymi, som forsøgte at gøre billige metaller som bly og kobber til guld, endnu ikke er lykkedes. Imidlertid, med udviklingen af legerin -
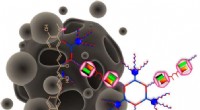 Forskere opdager metode til at levere urtetilskud curcumin til kræftceller ved at løse dets uoplø…Holdet detaljerede en hierarkisk tilgang til at solubilisere et hydrofobt anti-cancer lægemiddel, curcumin i vand via en kombination af koordinationsdrevet selvsamling og vært-gæst interaktioner. Kred
Forskere opdager metode til at levere urtetilskud curcumin til kræftceller ved at løse dets uoplø…Holdet detaljerede en hierarkisk tilgang til at solubilisere et hydrofobt anti-cancer lægemiddel, curcumin i vand via en kombination af koordinationsdrevet selvsamling og vært-gæst interaktioner. Kred -
 Garn belagt med enzymer kan fungere som filtreOrange biokatalytisk garn med iltbobler. Kredit:Lynn Doby, multimedie specialist, Tekstiler kreative og teknologiske tjenester, Wilson College of Textiles, NC stat. North Carolina State University
Garn belagt med enzymer kan fungere som filtreOrange biokatalytisk garn med iltbobler. Kredit:Lynn Doby, multimedie specialist, Tekstiler kreative og teknologiske tjenester, Wilson College of Textiles, NC stat. North Carolina State University
- Antallet af valenselektroner i gallium?
- Undervisning i CRISPR og antibiotikaresistens til gymnasieelever
- Hvad er forskellen mellem sammensætning og fysiske jordlag?
- Hvor mange atomer i natriumsulfid?
- Hvilken planet kan kun ses på nattehimlen med et teleskop?
- En større undersøgelse finder, at mange planlagte veje i troperne ikke burde bygges


