Beregning af osmolaritet:En trin-for-trin guide til nøjagtige løsninger
artisteer/iStock/GettyImages
Osmolaritet er et mål for koncentrationen af et opløst stof i en opløsning. Det er specifikt et mål for antallet af mol opløste partikler i et givet volumen opløsning og ligner molaritet, som måler antallet af mol opløst stof i et givet volumen opløsning. Osmolaritet kan beregnes ud fra den osmotiske koefficient, antallet af partikler, som det opløste stof dissocierer i, og molariteten af det opløste stof.
Trinnene
Trin 1
Beskriv forskellen mellem osmolaritet og molaritet. Denne sondring skyldes det faktum, at nogle opløste stoffer dissocierer, når de opløses, mens andre ikke gør det. For eksempel opløses bordsalt (NaCl) i dets komponentioner (Na+ og Cl-), når det opløses. På den anden side dissocierer glucose ikke til mindre partikler, når det opløses.
Trin 2
Definer osmolaritetsenhederne. Osmolaritet måles i osmol opløst stof pr. liter opløsning (osmol/L). En osmol kan uformelt beskrives som antallet af mol af opløste bestanddele i en opløsning.
Trin 3
Beskriv den osmotiske koefficient. Denne værdi er en testløsnings afvigelse fra den ideelle løsning. Den komplette beregning af den osmotiske koefficient er kompleks, men det er graden af dissociation af det opløste stof for simple tilfælde. Den osmotiske koefficient vil derfor have et interval på 0 til 1 i disse tilfælde, således at den osmotiske koefficient vil være 1, når det opløste stof er fuldstændigt opløst.
Trin 4
Beregn osmolariteten ud fra observerede værdier. En opløsnings osmolaritet kan angives som summen af (yi)(ni)(Ci), hvor yi er den osmotiske koefficient for opløst stof i, n er antallet af partikler, som opløst stof i dissocierer i, og Ci er molariteten af opløst stof i.
Trin 5
Mål osmolaritet direkte med et osmometer. Disse enheder måler osmolariteten af specifikke partikler, såsom dem, der reducerer damptrykket af en opløsning eller sænker frysepunktet for en opløsning.
 Varme artikler
Varme artikler
-
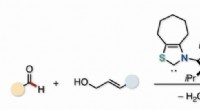 Partnere i katalyse:En effektiv vej til umættede ketonerDen samvirkende virkning af en organokatalysator og en palladiumkatalysator muliggjorde en første dehydrerende direkte allylering mellem aldehyder og allylalkoholer for at producere β, γ-umættede keto
Partnere i katalyse:En effektiv vej til umættede ketonerDen samvirkende virkning af en organokatalysator og en palladiumkatalysator muliggjorde en første dehydrerende direkte allylering mellem aldehyder og allylalkoholer for at producere β, γ-umættede keto -
 Påvisning af metabolitter på tæt holdKAUST-forskere har udviklet en biosensor, der kan tilpasses i en transistorkonfiguration i mikronskala for at detektere enhver metabolit af interesse. Kredit:2018 KAUST Et nyt koncept for en biose
Påvisning af metabolitter på tæt holdKAUST-forskere har udviklet en biosensor, der kan tilpasses i en transistorkonfiguration i mikronskala for at detektere enhver metabolit af interesse. Kredit:2018 KAUST Et nyt koncept for en biose -
 Højteknologisk gel hjælper med levering af lægemidlerGel hjælper med levering af lægemidler. Kredit:Eben Alsberg Lægemidler, der hjælper med at forhindre dannelsen af uønskede eller skadelige proteiner, er i øjeblikket ved at blive udviklet til at
Højteknologisk gel hjælper med levering af lægemidlerGel hjælper med levering af lægemidler. Kredit:Eben Alsberg Lægemidler, der hjælper med at forhindre dannelsen af uønskede eller skadelige proteiner, er i øjeblikket ved at blive udviklet til at -
 Forskere skaber syntetisk prototissue, der kan synkroniseresOpdagelsen, udgivet i Naturmaterialer , er den første kemisk programmerede tilgang til fremstilling af et kunstigt væv. Fundene, som kan have store sundhedsmæssige anvendelser i fremtiden, kunne se
Forskere skaber syntetisk prototissue, der kan synkroniseresOpdagelsen, udgivet i Naturmaterialer , er den første kemisk programmerede tilgang til fremstilling af et kunstigt væv. Fundene, som kan have store sundhedsmæssige anvendelser i fremtiden, kunne se
- Undersøgelse understreger nye strategier til at bekæmpe medicinresistente bakterier
- Er fosfortrihydrid en ionisk eller en kovalent binding?
- Forskere genbruger MRI-magnet til nye opdagelser
- Pennsylvania korrelerer fracking af naturgas med jordskælv
- En verdens første inden for cirkadisk urmanipulation
- Hvad er forskellen mellem arkæologi og gravrøveri?


