Konverter vandets hårdhed fra mg/L til Grains Per Gallon (GPG) – en trin-for-trin guide
Af David Robinson • Opdateret 24. marts 2022
Vandets hårdhed er defineret af mængden af opløste calcium- og magnesiumioner, det indeholder. Disse polyvalente kationer opstår, når vand passerer gennem kalkholdige formationer som kalksten, og de påvirker, hvordan vandet reagerer med rengøringsmidler, sæber og andre kemikalier. Hårdt vand har høje kationniveauer, hvorimod blødt vand indeholder forholdsvis lave koncentrationer. Kationkoncentrationer udtrykkes almindeligvis enten som korn pr. gallon (GPG) eller milligram pr. liter (mg/L).
Trin 1 – Identificer mg/L-værdien
Start med at bestemme vandets hårdhed i mg/L. Indtast tallet i en lommeregner, og dobbelttjek, at tallet er korrekt.
Trin 2 – Konverter til GPG
Divider mg/L-tallet med 17,2, standardomregningsfaktoren. Resultatet, afrundet til én decimal, giver hårdheden i GPG.
Trin 3 – Bekræft resultatet
For at bekræfte nøjagtigheden skal du gange GPG-værdien med 17,1. Hvis produktet ikke er tæt på det originale mg/L-tal, gentages beregningen.
TL;DR
mg/L x 17,1 ≈ GPG; GPG ÷17,2 ≈ mg/L.
Bemærk:1 mg/L er lig med 1 ppm, fordi et kilogram vand indeholder en million milligram.
 Varme artikler
Varme artikler
-
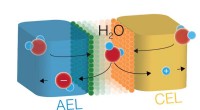 Forskere adskiller vand effektivt med nye katalysatorerForskning i et kemilaboratorium fra University of Oregon har fremskyndet effektiviteten af den katalytiske vanddissociationsreaktion i bipolære membraner. Et team på tre medlemmer brugte en membran-
Forskere adskiller vand effektivt med nye katalysatorerForskning i et kemilaboratorium fra University of Oregon har fremskyndet effektiviteten af den katalytiske vanddissociationsreaktion i bipolære membraner. Et team på tre medlemmer brugte en membran- -
 Se mere med PET-scanninger:Overraskende ny mekanisme til at fastgøre kemiske sporstoffer opdagetPositron emission tomografi/computertomografi (PET/CT) scanner. Kredit:Wikimedia Commons Forskere har fundet en overraskende alsidig løsning til at skabe kemiske forbindelser, der kan vise sig nyt
Se mere med PET-scanninger:Overraskende ny mekanisme til at fastgøre kemiske sporstoffer opdagetPositron emission tomografi/computertomografi (PET/CT) scanner. Kredit:Wikimedia Commons Forskere har fundet en overraskende alsidig løsning til at skabe kemiske forbindelser, der kan vise sig nyt -
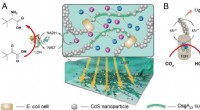 Bakteriebiofilm letter biokompatible bio-abiotiske grænseflader til semi-kunstig fotosynteseFig. 1. Skematisk af levende bio-abiotiske grænseflader for enkelt enzym til helcelle fotokatalyse. Kredit:SIAT Semi-kunstig fotosyntese integrerer den høje selektivitet af levende biosystemer og d
Bakteriebiofilm letter biokompatible bio-abiotiske grænseflader til semi-kunstig fotosynteseFig. 1. Skematisk af levende bio-abiotiske grænseflader for enkelt enzym til helcelle fotokatalyse. Kredit:SIAT Semi-kunstig fotosyntese integrerer den høje selektivitet af levende biosystemer og d -
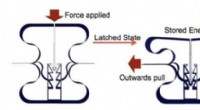 Forskere designer materiale, der kan lagre energi som et ørnegrebDen skraldende byggeklods, der kunne indlejres i de nye materialer. Efter lodret kompression, det holder materialer kollapset, og kan frigive deres energi på side-vejs pull. Kredit:Stoyan Smoukov
Forskere designer materiale, der kan lagre energi som et ørnegrebDen skraldende byggeklods, der kunne indlejres i de nye materialer. Efter lodret kompression, det holder materialer kollapset, og kan frigive deres energi på side-vejs pull. Kredit:Stoyan Smoukov
- Hvad er nogle vigtige anvendelser af svovl?
- Fremtidige klimapåvirkninger bringer pukkelhvalens kost i fare
- Hvilken energi overføres, når træ brændt?
- Hvor mange kerneelektroner i nitrogen?
- Forklar den effekt, som tyngdekraften har på hastigheden af faldende genstande?
- Olivenmøllens spildevand omdannet:Fra forurenende stof til biogødning, biobrændstof


