Forståelse af Tungsten Bonding:Metallisk struktur og kemiske forbindelser
Af John Brennan
Opdateret 24. marts 2022
Wolfram (atomnummer 74) er et tæt, gråt metal kendt for sit usædvanligt høje smeltepunkt og fremragende mekaniske egenskaber. Mens dens mest velkendte rolle er i glødepæreglødetråde, stammer dens industrielle betydning i høj grad fra produktionen af wolframcarbid og dets anvendelse i højtemperaturlegeringer. Kernen i disse applikationer ligger arten af de bindinger, der holder wolframatomer sammen.
Elektronkonfiguration
I sin isolerede grundtilstand har et wolframatom den elektroniske konfiguration [Xe]4f 14 5d 4 6s 2 . Men når atomer pakker sig ind i et krystalgitter, skifter energiniveauerne:5d sub-skallen bliver fuldt optaget (fem elektroner), mens 6s sub-skallen rummer en enkelt elektron. 5d-elektronerne er i stand til at danne retningsbestemte, kovalente interaktioner, der er relativt lokaliserede mellem naboatomer, hvorimod 6s-elektronerne delokaliseres hen over gitteret.
Metallisk binding
I fast tilstand opfører de delokaliserede 6s elektroner sig som et "hav" af mobil ladning, der gennemsyrer metallet. Denne elektrongas binder de positivt ladede wolframkerner sammen, hvilket giver materialet dets karakteristiske metalliske binding. Overlapningen af mange atomare orbitaler skaber et tæt bånd af energiniveauer, som elektroner kan optage, hvilket forklarer wolframs høje elektriske ledningsevne og dets modstand mod deformation.
Krystalstruktur og fysiske egenskaber
Wolfram krystalliserer i flere allotroper:den mest almindelige er den kropscentrerede kubiske alfafase, som er den mest termodynamisk stabile. Der eksisterer også en betafase med høj temperatur; ved afkøling omdannes betastrukturen til alfa. Den metalliske binding, kombineret med en tæt pakning af atomer, resulterer i et metal, der er både formbart og duktilt - typiske træk ved metaller, hvor atomer ikke er låst fast i et stift gitter som diamant.
Wolframforbindelser
Når wolfram reagerer med ikke-metalliske grundstoffer eller ligander, danner det koordinationskomplekser og kovalente forbindelser. Disse bindingers del-elektronkarakter står i kontrast til den metalliske binding i det elementære metal. Wolframs oxidationstilstande i sådanne forbindelser varierer fra -2 til +6, hvilket afspejler mangfoldigheden af dets kemi. Ved forhøjede temperaturer oxiderer wolfram let; det er derfor, glødepærer er fyldt med inaktive gasser - for at forhindre nedbrydning af glødetråden.
Sidste artikelSådan svejses stålrør:En trin-for-trin guide
Næste artikelHårdt vs. blødt vand:nøgleforskelle og hvordan de påvirker dit liv
 Varme artikler
Varme artikler
-
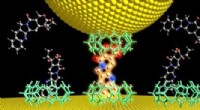 Forskere udvikler ny målemetode inden for molekylær elektronikGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202203830 I molekylær elektronik strækkes enkelte molekyler mellem to elektroder for at danne et elektrisk
Forskere udvikler ny målemetode inden for molekylær elektronikGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202203830 I molekylær elektronik strækkes enkelte molekyler mellem to elektroder for at danne et elektrisk -
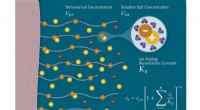 Forskning beskriver, hvordan ioner spiller en nøglerolle i at kontrollere slimhindeoverfladerKredit:KC Jones (Keck Graduate Institute) To nylige artikler fra Keck Graduate Institute (KGI) professor James Sterling og Shenda Baker, President og COO hos Synedgen, beskrive hvordan ioner inter
Forskning beskriver, hvordan ioner spiller en nøglerolle i at kontrollere slimhindeoverfladerKredit:KC Jones (Keck Graduate Institute) To nylige artikler fra Keck Graduate Institute (KGI) professor James Sterling og Shenda Baker, President og COO hos Synedgen, beskrive hvordan ioner inter -
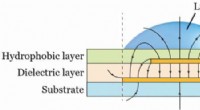 Hydrogel 3-D udskrivning og mønster af væsker med kondensatorkanteffekten (PLEEC)Princippet om PLEEC. En asymmetrisk kondensator er adskilt af et dielektrisk lag. Kredit:Science Advances, doi:10.1126/sciadv.aau8769 Hydrogeler er tredimensionelle (3-D) polymernetværk, der kan t
Hydrogel 3-D udskrivning og mønster af væsker med kondensatorkanteffekten (PLEEC)Princippet om PLEEC. En asymmetrisk kondensator er adskilt af et dielektrisk lag. Kredit:Science Advances, doi:10.1126/sciadv.aau8769 Hydrogeler er tredimensionelle (3-D) polymernetværk, der kan t -
 Bakteriefilm adskiller vand fra olieBakteriel cellulose viste nytte til at adskille olie og vand i eksperimenter ledet ved NC State. Kredit:Zahra Ashrafi Forskere har påvist, at en slimet, dog hård, type biofilm, som visse bakterier
Bakteriefilm adskiller vand fra olieBakteriel cellulose viste nytte til at adskille olie og vand i eksperimenter ledet ved NC State. Kredit:Zahra Ashrafi Forskere har påvist, at en slimet, dog hård, type biofilm, som visse bakterier
- Hvordan biometan kan hjælpe med at gøre gas til en vedvarende energikilde
- Hvor er Mars relation til jorden?
- Delvis solformørkelse synlig over hele Storbritannien
- Hvem har vedtaget permanent dagslysbesparelser i kraft hele året rundt?
- Klimabeskyttelse og ren luft:En integreret tilgang
- Nye beviser på omstridt identitet af middelalderskelet fundet ved Prags slot


