Hårdt vs. blødt vand:nøgleforskelle og hvordan de påvirker dit liv
Af Rosann Kozlowski Opdateret 24. marts 2022
pinkomelet/iStock/GettyImages
Vand kan nogle gange beskrives som værende hårdt vand og blødt vand. Forskellen hviler på mængden af opløste mineraler i vandet. Hårdt vand indeholder en høj mængde mineraler, og blødt vand indeholder kun lidt eller ingen.
Hårdt vand og blødt vand:Oprindelse
Hårdt vand og blødt vand:Oprindelse
Vand akkumulerer opløste faste stoffer, når det bevæger sig gennem klipper og andre substrater, såsom kalksten, gips eller dolomit. Calcium og magnesium er særligt opløselige i vand, og hvis disse naturligt forekommende mineraler er inden for det geografiske område, vil beboerne omkring vandkilden have hårdt vand .
I USA har områder af østkysten generelt blødt vand, og dem i sydvest har hårdt vand. Regnvand anses for blødt, eftersom det ikke er trængt gennem jordstoffer, som grundvand har gjort.
Hårdt vand og blødt vand:niveauer
Hårdt vand og blødt
Vand:Niveauer
Karakteristikaene for hårdt vand og blødt vand er bestemt af mængden af mineraler i vand, målt i milligram per liter eller i korn per gallon. Hårdhed afhænger også af vandets pH og temperatur.
De amerikanske nationale standarder definerer blødt vand som indeholdende mindre end 17,1 mg/L; dog kan følgende niveauer bruges til at tilnærme vandhårdheden:
- Blødt:0 – 60 mg/L
- Moderat hård:61
– 120 mg/L* Hård:121 – 180 mg/L
- Meget hårdt:181 mg/L og derover
Kemiske egenskaber ved HardWater
Kemiske egenskaber af Hard
Vand
Almindelige bidragydere til vandhårdhed er calcium, Ca og magnesium, Mg. Begge grundstoffer er jordalkalimetaller, der findes i gruppe 2 i det periodiske system. Grundstofferne i gruppe 2-søjlen har en 2+ ladning og mister to elektroner for at danne kationer, såsom Ca2+ og Mg2+. Disse kationer opløses let i vand.
Calciumcarbonat , CaCO3 er et almindeligt stof i bjergarter, især af kalksten, en type sedimentær bjergart og dolomit, CaMg(CO3)2, også en sedimentær bjergart. Calciumcarbonat findes også i skallerne på marine organismer og æg.
Når regnvand med opløst kuldioxid, CO2, filtreres gennem calciumcarbonat, opløses calciumionerne i vandet. Følgende kemiske ligning beskriver denne proces:
CaCO3(s) + H20(l) + CO2(aq) → Ca2+(aq) + 2HCO3-
Hvor calciumcarbonatet, CaCO3, danner Ca2+ og bicarbonat, HCO3-, i nærværelse af vand og kuldioxid.
Typer af hårdt vand
Typer af hårdt vand
Egenskaberne ved hårdt vand beskrives som midlertidige og permanente . Midlertidigt hårdt vand indeholder bicarbonat, HCO3-. Permanent hårdt vand indeholder bicarbonationer med andre ioner som sulfat, SO42-. Kogning udfælder ikke de permanent hærdende arter, og natriumcarbonat, Na2CO3, vil skulle tilsættes.
Hårdt vands egenskaber:Dannelse af bundfald
Hårdt vands egenskaber:Dannelse
Udfældninger
Når hårdt vand opvarmes, efterlader det ofte en belægning på gryder eller beholdere. Bemærk, at ligningen for dette bundfald er den omvendte for Ca2+-ionerne, der opløses i vandig opløsning:
Ca2+(aq) + 2HCO3- (aq) → CaCO3(s) + H20 (l) + CO2(aq)
Calciumcarbonatbundfaldet, CaCO3, kaldes kedelsten. Selvom det er frustrerende at gøre rent, er det ikke et sundhedsproblem.
Bundfaldet kan bygge sig over tid; dog, og dette kan påvirke levetiden for apparater som opvaskemaskiner og vaskemaskiner og eventuelle VVS-rør. Opbygningen indsnævrer det rum, hvor vandet kan strømme, og apparater og rør skal udskiftes.
Hårdt vands egenskaber:Overfladeaktivt stofinterferens
Hårdt vands egenskaber:
Surfaktantinterferens
Som nævnt ovenfor indeholder hårdt vand opløste mineraler, der kan give problemer for forbrugerne ved at efterlade aflejringer i VVS og apparater. Hårdt vand forstyrrer også effektiviteten af mange husholdningsrengøringsprodukter.
Ca2+- og Mg2+-ionerne interfererer med **sæbens overfladeaktive kvaliteter. ** Et overfladeaktivt middel sænker vandets overfladespænding, så det kan bevare kontakten med en fast overflade, såsom tøj eller en håndvask. Ionerne forstyrrer det overfladeaktive stofs proces, og dette kræver ofte ekstra vaske- eller rengøringsmiddel for at fuldføre en opgave.
Mineralerne i hårdt vand kombineres også med sæbe for at lave en klistret eller uklar hinde på service og i badekar, brusere og håndvaske. Denne film kan også overtrække tøj, hud og hår, få tøjet til at virke snusket og forårsage tør eller irriteret hud eller hår, der er kedeligt og uhåndterligt.
Fordele med hårdt vand og blødt vand
Hårdt vand og blødt vand
Fordele
Hårdt vand har en ekstra sundhedsfordel. Calcium og magnesium er vigtige mineraler, som kroppen har brug for til vækst og funktion af knogler og muskler. Disse mineraler regulerer også blodtryk og enzymhandlinger. Indtagelse af hårdt vand kan være en kilde til disse mineraler.
Blødt vand har ikke de negative virkninger af mineralaflejringer på husholdningsapparater og VVS-rør. Den mangler mineralsk smag af hårdt vand og efterlader ikke rester på hud, fade eller andre overflader.
Metoder til blødgøring af hårdt vand
Metoder til blødgøring af hårdt vand
Et husholdningsblødgøringsanlæg virker ved ionbytning. Når det hårde vand ledes gennem en ionbytter, flyder det af lag af polymer (plastik) perler, der er kovalent bundet til aniongrupper, såsom:
- –COO-
- natrium
- Na+
- eller kalium
- K+ kationer
Når vandet passerer forbi disse perler, fortrænger calcium- og magnesiumionerne natrium- eller kaliumionerne.
Blødgøringsmidler:Fordele
Blødgøringsmidler:Fordele
Fordelene ved blødgøringsmidler er renere vasketøj, apparater med længere holdbarhed og ingen klæbrig sæbe. Forbrugerne bruger mindre vaskemiddel og andre typer rengørings- og vaskemidler. Tøj er lysere, og håndvaske, badekar og brusere kræver mindre rengøring.
Vandapparater som kedler, vandvarmere og opvaskemaskiner kører typisk mere effektivt og behøver mindre vedligeholdelse, da blødt vand ikke forårsager kalkopbygning i rør og VVS-armaturer. Brugere af blødt vand rapporterer ofte, at hår og hud føles mindre tørre og skællet.
Blødgøringsmidler:Ulemper
Blødgøringsmidler:Ulemper
Ulemperne ved blødgøringsmidler omfatter de høje omkostninger og indsats, der er forbundet med at vedligeholde et vandblødgørende system. Et blødgøringsanlæg og dets installation kan koste tusindvis af amerikanske dollars, og vandblødgøringsalt skal tilsættes regelmæssigt.
Vandblødgøringsmidler er vandintensive i regenereringsprocessen og bruger op til 25 liter vand om dagen. Skylning af blødgøringsmidler med en saltopløsning kan have en negativ indvirkning på miljøet. Dette vand, med dets høje natriumindhold, anbefales ikke til vanding af planter, græsplæner eller haver.
Sundhedsmæssigt indeholder blødgjort vand mere natrium end hårdt vand, og det kan være problematisk for folk, der skal begrænse deres saltindtag i kosten. Fordi meget af calcium og magnesium er blevet fjernet, er blødt vand ikke en kilde til disse mineraler i kosten.
 Varme artikler
Varme artikler
-
 En nanoteknologisk sensor, der forvandler molekylære fingeraftryk til stregkoderForfatterne viser en pixeleret sensormetasurface til molekylær spektroskopi. Den består af metapixels designet til at koncentrere lys til nanometerstore volumener for at amplificere og detektere absor
En nanoteknologisk sensor, der forvandler molekylære fingeraftryk til stregkoderForfatterne viser en pixeleret sensormetasurface til molekylær spektroskopi. Den består af metapixels designet til at koncentrere lys til nanometerstore volumener for at amplificere og detektere absor -
 Forskere udvikler en procedure og en billig, hurtig og miljøvenlig enhed, der er i stand til at det…Kredit:Alicante University Alicante Universitets analytiske atomspektrometri forskergruppe ledet af analytisk kemiprofessor Juan Mora Pastor, har udviklet en ny procedure og enhed til at detektere
Forskere udvikler en procedure og en billig, hurtig og miljøvenlig enhed, der er i stand til at det…Kredit:Alicante University Alicante Universitets analytiske atomspektrometri forskergruppe ledet af analytisk kemiprofessor Juan Mora Pastor, har udviklet en ny procedure og enhed til at detektere -
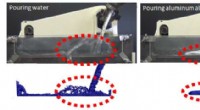 Forskere kopierer hældningsadfærd for smeltet metal med nyudviklet simuleringsteknologiFigur:Prøvning af simuleringsteknologien i sammenligning med et hældeforsøg med Die Casting shot sleeves:Simuleringen (nedenfor) replikerer korrekt forskellene i bevægelse af vand og aluminiumlegering
Forskere kopierer hældningsadfærd for smeltet metal med nyudviklet simuleringsteknologiFigur:Prøvning af simuleringsteknologien i sammenligning med et hældeforsøg med Die Casting shot sleeves:Simuleringen (nedenfor) replikerer korrekt forskellene i bevægelse af vand og aluminiumlegering -
 Video:Hvorfor ændrer salt smagen af alting?Kredit:The American Chemical Society Hvis din kaffe er for bitter, tilsæt en knivspids salt. Hvis din salat ikke er sur nok, tilsæt et nip salt. Hvis din øl er for bitter, tilsæt en knivspids salt.
Video:Hvorfor ændrer salt smagen af alting?Kredit:The American Chemical Society Hvis din kaffe er for bitter, tilsæt en knivspids salt. Hvis din salat ikke er sur nok, tilsæt et nip salt. Hvis din øl er for bitter, tilsæt en knivspids salt.
- Når klipper bryder, hvad hedder det, når de flytter?
- Graphen sætter sit præg på gasseparation
- Hvilken slags materiale er krysotil?
- Sådan finder du alle fakta af et nummer hurtigt og nemt
- Hvordan producerer og frigiver en celle protein?
- Hvorfor er elektronmikroskop en fordel, når man studerer celler?


