Tre nøgleegenskaber ved ioniske forbindelser
Af Drew Lichtenstein Opdateret 24. marts 2022
En forbindelse er et stof dannet ved at kombinere to eller flere forskellige atomer. Når disse atomer holdes sammen af den elektrostatiske tiltrækning mellem modsat ladede ioner, er det resulterende materiale en ionisk forbindelse.
Definition
Ioniske forbindelser består af mindst et metal og et ikke-metal. En ion dannes, når et atom taber eller får elektroner og får en positiv eller negativ ladning. Ionbindingen er en kraftig tiltrækning mellem disse ladede arter.
Solid State ved stuetemperatur
På grund af deres stærke ionbindinger er disse materialer faste under almindelige forhold. De udviser en stiv gitterstruktur, som tegner sig for deres høje smelte- og kogepunkter. Et velkendt eksempel er bordsalt (NaCl), som krystalliserer til et kubisk gitter af Na⁺- og Cl⁻-ioner. Mens ioniske forbindelser ofte er opløselige i vand, ændrer opløselighed ikke deres faste tilstand.
Metallige egenskaber
Mange ioniske faste stoffer udviser metallignende egenskaber:de reflekterer lys (glans), har høje tætheder og leder varme og elektricitet, når de er smeltet eller opløst, selvom deres faststofledningsevne er forholdsvis lav.
Stabile ioniske bindinger og termiske egenskaber
Den energi, der holder ioner sammen i gitteret, kaldes gitterenergi. Denne robuste binding gør ioniske forbindelser modstandsdygtige over for ændringer, hvilket resulterer i smeltepunkter, der kan nå flere hundrede grader celsius og kogepunkter langt over kovalente molekylers.
At forstå disse egenskaber – fast struktur, metalliske egenskaber og stærk ionbinding – giver indsigt i, hvorfor ioniske forbindelser opfører sig, som de gør i daglig kemi.
 Varme artikler
Varme artikler
-
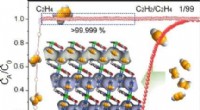 Adskillelse af sporacetylen fra ethylen i ultramikroporøse metal-organiske rammerKredit:Angewandte Chemie Ethylen, en vigtig råvare i den kemiske industri, indeholder ofte spor af acetylenforureninger, som skal fjernes. I journalen Angewandte Chemie , forskere beskriver en r
Adskillelse af sporacetylen fra ethylen i ultramikroporøse metal-organiske rammerKredit:Angewandte Chemie Ethylen, en vigtig råvare i den kemiske industri, indeholder ofte spor af acetylenforureninger, som skal fjernes. I journalen Angewandte Chemie , forskere beskriver en r -
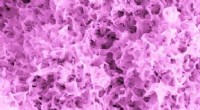 Proteiner koreograferer den uendelig lille dans af levende celler og funktionelle biomaterialerBlomsterlignende mikrostrukturer dannes på en nanoporøs glasmonolit med 31nm-diameter porer. Kredit:Lehigh University, Thamma, Kowal, Falk, Jain Et tværfagligt forskerhold ved Lehigh University ha
Proteiner koreograferer den uendelig lille dans af levende celler og funktionelle biomaterialerBlomsterlignende mikrostrukturer dannes på en nanoporøs glasmonolit med 31nm-diameter porer. Kredit:Lehigh University, Thamma, Kowal, Falk, Jain Et tværfagligt forskerhold ved Lehigh University ha -
 Ny sensor kan snart teste for coronavirus og influenza samtidigtDenne sensor er på størrelse med et mikro-USB-drev og er i stand til at teste for influenza og COVID-19 samtidigt. Kredit:Dmitry Kireev, University of Texas i Austin Den nye coronavirus er blevet
Ny sensor kan snart teste for coronavirus og influenza samtidigtDenne sensor er på størrelse med et mikro-USB-drev og er i stand til at teste for influenza og COVID-19 samtidigt. Kredit:Dmitry Kireev, University of Texas i Austin Den nye coronavirus er blevet -
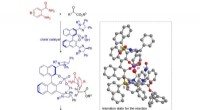 Ny metode til asymmetrisk N, N-acetalsyntese lover fremskridt inden for lægemiddeludviklingKredit:Nagoya Institute of Technology Mange af vores lægemidler og andre bioaktive lægemidler er baseret på kemiske strukturer kaldet enantiomerer - molekyler, der er spejlbilleder af hinanden og
Ny metode til asymmetrisk N, N-acetalsyntese lover fremskridt inden for lægemiddeludviklingKredit:Nagoya Institute of Technology Mange af vores lægemidler og andre bioaktive lægemidler er baseret på kemiske strukturer kaldet enantiomerer - molekyler, der er spejlbilleder af hinanden og
- Tid, sted og hvordan træ bruges er faktorer i kulstofemissioner fra skovrydning
- Uber går sammen med det japanske taxafirma for at knække hårde markeder
- Hvilke materialer kan vibrationer rejse igennem?
- Jordskred-ur:Kan eksperter forudsige kollaps ved Washingtons Rattlesnake Ridge?
- Hvis en eukaryotisk celle laver anaerob respiration, hvor mange fødevaremolekyler ville det være n…
- Sådan beregnes en T-score


