Hvor meget vand skal der til for at opløse bordsalt? En praktisk guide
Af Natalie Andrews – Opdateret 24. marts 2022
ArtCookStudio/iStock/GettyImages
Ved stuetemperatur (ca. 25°C) kan en standard 100 g (≈100 ml) vand opløse ca. 35 g natriumchlorid (bordsalt). Denne værdi repræsenterer opløselighedsgrænsen; eventuelt yderligere salt vil forblive på bunden af beholderen, hvilket indikerer en mættet opløsning.
Hvordan temperatur påvirker opløseligheden
Opløseligheden af de fleste faste stoffer stiger med temperaturen, selvom størrelsen varierer efter forbindelse. For natriumchlorid er stigningen beskeden:ved 100°C stiger opløseligheden til omkring 39 g pr. 100 g vand, hvilket tillader et par gram mere salt at opløses, før mætning er nået.
Varmt vand
Når vandet er tæt på kogepunktet, kan det rumme op til ~40 g salt før mætning, hvilket forklarer, hvorfor kokke ofte tilføjer en knivspids salt til kogende vand for at fremskynde tilberedningen.
Koldt vand
Under koldere forhold opløses salt langsommere, og tilstedeværelsen af salt sænker vandets frysepunkt - et fænomen kendt som frysepunktsdepression. Tilsætning af salt til is forhindrer effektivt isen i at smelte, et princip, der udnyttes ved afisning af veje.
Mættede vs. umættede løsninger
En umættet opløsning indeholder mere tilgængeligt opløsningsmiddel end opløst stof; saltkrystaller er fuldt hydrerede og opløses fuldstændigt. En mættet Opløsningen har nået ligevægt:opløsningshastigheden er lig med krystallisationshastigheden, og eventuelt ekstra salt vil simpelthen bundfælde sig.
Under det normale frysepunkt – omkring –6 °C (–5,98 °F) – kan vand ikke længere acceptere yderligere saltmolekyler. Blandingen består så af faste iskrystaller spækket med saltkorn.
Effekt af salttype
Ikke alle salte opfører sig identisk. Stensalt, som indeholder urenheder, opløses langsommere end rent bord- eller konservesalt. Tilstedeværelsen af mineraler eller tilsætningsstoffer kan forstyrre hydreringsprocessen og forlænge den tid, der kræves for fuld opløsning.
 Varme artikler
Varme artikler
-
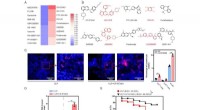 PDGFR-kinasehæmmer fundet at beskytte mod septisk død via regulering af BTLAA, Heatmap, der afbilder virkningen af lægemiddelbiblioteksinhibitorer på ekspressionsniveauet af BTLA i RAW264.7-celler ved in-celle western blotting. De 10 bedste lægemidler, der hæmmer (venstre)
PDGFR-kinasehæmmer fundet at beskytte mod septisk død via regulering af BTLAA, Heatmap, der afbilder virkningen af lægemiddelbiblioteksinhibitorer på ekspressionsniveauet af BTLA i RAW264.7-celler ved in-celle western blotting. De 10 bedste lægemidler, der hæmmer (venstre) -
 Plasmaprotein kan holde løfte om sårstilladserKredit:CC0 Public Domain Forskere i Tyskland har ansat et plasmaprotein, der findes i blod, til at udvikle en ny metode til fremstilling af sårhelende vævsstilladser. Teamets nye stillads kan fas
Plasmaprotein kan holde løfte om sårstilladserKredit:CC0 Public Domain Forskere i Tyskland har ansat et plasmaprotein, der findes i blod, til at udvikle en ny metode til fremstilling af sårhelende vævsstilladser. Teamets nye stillads kan fas -
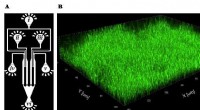 Vask genstridige biofilm væk ved hjælp af svampe rengøringsmidlerKredit:University of Tsukuba Lurer inde i rør og på overflader af medicinsk udstyr, slimede lag af bakterier, kaldet biofilm, forårsage problemer lige fra storskala produktkontaminering til potent
Vask genstridige biofilm væk ved hjælp af svampe rengøringsmidlerKredit:University of Tsukuba Lurer inde i rør og på overflader af medicinsk udstyr, slimede lag af bakterier, kaldet biofilm, forårsage problemer lige fra storskala produktkontaminering til potent -
 Forskere kommer op med en hurtigere måde at opdage antibiotika påKredit:Elena Khavina/MIPT Pressekontor Russiske biokemikere har identificeret en lovende ny klasse af antibiotika. Efter at have studeret over 125, 000 molekyler, de fandt, at 2-pyrazol-1-yl-thiaz
Forskere kommer op med en hurtigere måde at opdage antibiotika påKredit:Elena Khavina/MIPT Pressekontor Russiske biokemikere har identificeret en lovende ny klasse af antibiotika. Efter at have studeret over 125, 000 molekyler, de fandt, at 2-pyrazol-1-yl-thiaz
- Hvad er fysisk -kemisk?
- Forskere afslører, hvordan grapefrugter udgør et hemmeligt våben til levering af lægemidler
- Direkte forberedelse af en ren bakteriekultur:Trin-for-trin-vejledning
- Den cykliske vej til ATP -dannelse fungerer hovedsageligt til?
- Hvad alle følgende er måder, hvorpå sedimentære klipper dannes undtagen A. lavakøling B. Fysisk…
- Hvordan fjernarbejde kan forårsage lederskabsproblemer for din virksomhed


