Ingeniører gør en ulempe - guld-nanopartiklernes klæbrighed - til en fordel
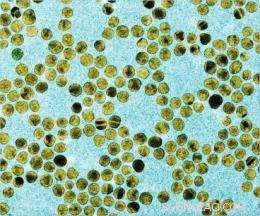
Et billede af guld nanopartikler. Billede udlånt af Kimberly Hamad-Schifferli
(PhysOrg.com) -- Guld nanopartikler -- bittesmå kugler af guld på kun et par milliardtedele meter i diameter -- er blevet nyttige værktøjer i moderne medicin. De er blevet indarbejdet i miniature-lægemiddelleveringssystemer for at kontrollere blodpropper, og de er også hovedkomponenterne i en enhed, nu i kliniske forsøg, der er designet til at brænde ondartede tumorer væk.
Imidlertid, en egenskab ved disse partikler står i vejen for mange nanoteknologiske udviklinger:De er klæbrige. Guld nanopartikler kan konstrueres til at tiltrække specifikke biomolekyler, men de holder sig også til mange andre utilsigtede partikler - hvilket ofte gør dem ineffektive til deres udpegede opgave.
MIT-forskere har fundet en måde at vende denne ulempe til en fordel. I et papir for nylig offentliggjort i American Chemical Society Nano , Lektor Kimberly Hamad-Schifferli fra Institut for Biologisk Teknik og Maskinteknik og postdoc Sunho Park PhD '09 fra Institut for Maskinteknik rapporterede, at de kunne udnytte nanopartiklernes klæbrighed til at fordoble mængden af protein produceret under in vitro-translation — en vigtig værktøj, som biologer bruger til sikkert at producere en stor mængde protein til undersøgelse uden for en levende celle.
Under oversættelsen grupper af biomolekyler samles for at producere proteiner fra molekylære skabeloner kaldet mRNA. In vitro translation udnytter de samme biologiske komponenter i et reagensglas (i modsætning til in vivo translation, som forekommer i levende celler), og et menneskeskabt mRNA kan tilsættes for at garantere produktionen af et ønsket protein. For eksempel, hvis en forsker ville studere et protein, som en celle ikke naturligt ville producere, eller et muteret protein, der ville være skadeligt for cellen in vivo, han kunne bruge in vitro-translation til at skabe store mængder af dette protein til observation og testning. Men der er en ulempe ved in vitro-oversættelse:Den er ikke så effektiv, som den kunne være. "Du får måske noget protein en dag, og ingen for de næste to, ” forklarer Hamad-Schifferli.
Med finansiering fra Institute of Biomedical Imaging and Bioengineering, Hamad-Schifferli og hendes medarbejdere satte sig oprindeligt for at designe et system, der ville forhindre oversættelse. denne proces, kendt som translationshæmning, kan stoppe produktionen af skadelige proteiner eller hjælpe en forsker med at bestemme proteinfunktionen ved at observere celleadfærd, når proteinet er blevet fjernet. For at opnå dette, Hamad-Schifferli knyttet DNA til guld nanopartikler, forventer, at de store nanopartikel-DNA (NP-DNA) aggregater ville blokere translation.
Hun var modløs, imidlertid, at finde ud af, at NP-DNA'et ikke reducerede proteinproduktionen som forventet. Faktisk, hun havde nogle foruroligende data, der tydede på, at i stedet for at hæmme oversættelse, NP-DNA'et booster det. "Det er, når vi tager vores tekniske kasketter på, ” husker Hamad-Schifferli.
Det viser sig, at de klæbrige nanopartikler bringer de biomolekyler, der er nødvendige for oversættelse, i umiddelbar nærhed, som hjælper med at fremskynde oversættelsesprocessen. Derudover DNA-delen af NP-DNA-komplekset er designet til at binde til et specifikt mRNA-molekyle, som vil blive oversat til et specifikt protein. Bindingen skal være tæt nok til at holde mRNA'et på plads til translation, men løst nok til, at mRNA'et også kan binde sig til de andre molekyler, der er nødvendige for processen. Fordi det designede DNA-molekyle har en specifik mRNA-partner, at mRNA i en opløsning af mange lignende molekyler kan forstærkes uden at skulle isoleres.
Ud over at forbedre in vitro-oversættelsen, Hamad-Schifferlis NP-DNA-komplekser kan have andre anvendelser. Ifølge Ming Zheng, en forskningskemiker ved National Institute of Standards and Technology, de kunne kombineres med kulstof nanorør - bittesmå, hule cylindre, der er utrolig stærke for deres størrelse. De kan i sidste ende være hjørnestenen i transportsystemer, der transporterer lægemidler ind i celler eller mellem celler. NP-DNA'ets klæbrighed kan øge hastigheden og nøjagtigheden af et sådant lægemiddelleveringssystem.
Selvom Hamad-Schifferli er overbevist om, at hendes opdagelse vil gøre in vitro-oversættelse mere pålidelig og effektiv, hun er ikke færdig. Hun håber at pille ved sit system for yderligere at øge proteinproduktionen in vitro, og se, om systemet kan anvendes til at forbedre translation i levende celler. For at hjælpe med at nå disse mål, hun skal designe og udføre eksperimenter for at bestemme, hvilke molekyler der er involveret i forbedringsprocessen, og hvordan de interagerer. "Fordelen er, at vi har været heldige, Hamad-Schifferli siger, reflekterer over hendes opdagelse. Ulempen er, at det vil være svært at afdække præcis, hvordan systemet fungerer.
 Varme artikler
Varme artikler
-
 Bærere leverer kontrollerbar kræftkemoterapiDisse mikroskopiske lægemiddelbærende pakker, kaldet nanovesikler, kunne give læger mulighed for præcist at kontrollere placeringen og tidspunktet for kemoterapilevering til tumorceller, ifølge ny IRP
Bærere leverer kontrollerbar kræftkemoterapiDisse mikroskopiske lægemiddelbærende pakker, kaldet nanovesikler, kunne give læger mulighed for præcist at kontrollere placeringen og tidspunktet for kemoterapilevering til tumorceller, ifølge ny IRP -
 Skånsomme sensorer til diagnosticering af hjernesygdommeGennem Polymer Vias-baseret 3D-integration forenkler vejen mod hjernemaskine-grænseflader med høj opløsning. Kredit:KAUST Fleksibel, billige sensorteknologi, der fører til sikrere og forbedrede di
Skånsomme sensorer til diagnosticering af hjernesygdommeGennem Polymer Vias-baseret 3D-integration forenkler vejen mod hjernemaskine-grænseflader med høj opløsning. Kredit:KAUST Fleksibel, billige sensorteknologi, der fører til sikrere og forbedrede di -
 Kemikere bliver molekylære billedhuggere, syntetisere lille, molekylære fælderEt illustreret tværsnit af et nanorør UB kemikere skabt. De grønne strukturer er negativt ladede carboxylsyregrupper, som hjælper med at fange positivt ladede partikler. (PhysOrg.com) -- Bruger sm
Kemikere bliver molekylære billedhuggere, syntetisere lille, molekylære fælderEt illustreret tværsnit af et nanorør UB kemikere skabt. De grønne strukturer er negativt ladede carboxylsyregrupper, som hjælper med at fange positivt ladede partikler. (PhysOrg.com) -- Bruger sm -
 Guldnanopartikler hjælper med at udvikle en ny metode til sporing af viraTil venstre:transmissionselektronmikroskopi (TEM) billede af et enkelt CVB3 -virus, der viser snesevis af guld nanopartikler fastgjort til dets overflade. Partiklerne danner et tydeligt mærkningsmønst
Guldnanopartikler hjælper med at udvikle en ny metode til sporing af viraTil venstre:transmissionselektronmikroskopi (TEM) billede af et enkelt CVB3 -virus, der viser snesevis af guld nanopartikler fastgjort til dets overflade. Partiklerne danner et tydeligt mærkningsmønst
- Glem at afrime din bil i et glacialt tempo:Ny forskning fremskynder processen tidoblet
- Simulerer 195 millioner år med globalt klima i mesozoikum
- Ny superledende magnet slår rekorder for magnetisk feltstyrke, baner vejen for fusionsenergi
- Massefremstilling af engangsansigtsskærme til Covid-19-respons
- Sådan finder du skråninger
- Hvorfor er det så svært at reducere afhængigheden af benzin?


