Billedstyret brystkræftbehandling muliggjort af nanodrug
Ved at kombinere en jernoxidnanopartikel, et tumor-målrettet peptid, og en terapeutisk nukleinsyre i én konstruktion, et team af efterforskere fra Massachusetts General Hospital og Harvard Medical School har skabt et middel, der rummer potentiale som målrettet behandling for brystkræft. Ud over, dette nye middel kan nemt spores i kroppen ved hjælp af standard magnetisk resonansbilleddannelse (MRI).
Zdravka Medarova ledede denne undersøgelse. Hun og hendes kolleger offentliggjorde deres resultater i tidsskriftet Kræftforskning .
Dr. Medarova og hendes samarbejdspartnere skabte deres nanopartikel for at binde til et tumorspecifikt molekyle kendt som uMUC-1, som findes på overfladen af over 90 procent af humane brysttumorer, og levere et syntetisk lille interfererende RNA (siRNA) molekyle designet til at lukke ned for et specifikt gen - BIRC5 - der blokerer celledød i de fleste tumorer og er forbundet med udvikling af lægemiddelresistens. Forskerne tilføjede også et fluorescerende farvestof til deres nanopartikel for at give dem mulighed for at spore nanopartiklerne ved hjælp af nær-infrarød spektroskopi. Fordi nanopartiklerne selv er sammensat af superparamagnetisk jernoxid, det er let synligt i MR-scanninger.
Når det tilsættes til brystkræftceller, der vokser i kultur, denne nanopartikelkonstruktion havde en dyb indvirkning på udtrykket af BIRC5 gen, slår dets udtryk ned. Både fluorescensbilleddannelse og MR viste, at nanopartiklerne blev optaget hurtigt af cellerne. Efterfølgende eksperimenter viste, at denne konstruktion havde den samme positive effekt på både humane bugspytkirtelkræftceller og tyktarmskræftceller.
Baseret på disse indledende resultater, forskerne injicerede nanopartiklerne intravenøst i mus med humane brysttumorer. Lægemidlet blev administreret ved to separate lejligheder, en uges mellemrum. Både MR- og fluorescensbilledscanninger afslørede, at nanopartiklerne fortrinsvis akkumulerede i tumorerne, og at tumorniveauerne forblev høje i løbet af to ugers eksperimentet. Meget lidt lægemiddel akkumuleret i muskelvæv omkring tumorerne.
Da selve tumorerne blev undersøgt, forskerne fandt ud af, at siRNA-nyttelasten gav en femdobling af celledød sammenlignet med, når dyrene i stedet blev behandlet med en lignende konstruktion, der bar et nonsens-siRNA-molekyle, selvom de to nanopartikler akkumulerede til samme niveau i tumorerne fra behandlede dyr. Dette resultat viser, at den terapeutiske effekt af konstruktionen er uafhængig af dens tumormålretningsegenskaber og i stedet er et resultat af dens terapeutiske siRNA-nyttelast.
 Varme artikler
Varme artikler
-
 Kunstig fotosyntese kan hjælpe med at lave brændstoffer, plast og medicinDen globale industrisektor tegner sig for mere end halvdelen af den samlede energiforbrug hvert år. Nu opfinder forskere et nyt kunstigt fotosyntetisk system, der en dag kan reducere industriens afh
Kunstig fotosyntese kan hjælpe med at lave brændstoffer, plast og medicinDen globale industrisektor tegner sig for mere end halvdelen af den samlede energiforbrug hvert år. Nu opfinder forskere et nyt kunstigt fotosyntetisk system, der en dag kan reducere industriens afh -
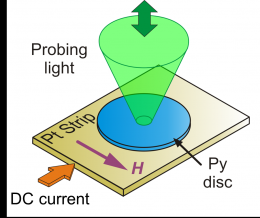 Team kontrollerer termiske udsving med spinstrøm(PhysOrg.com) - Et team af forskere fra NIST Center for Nanoscale Science and Technology, universitetet i Münster, og West Virginia University har demonstreret kontrol af magnetiske termiske fluktuati
Team kontrollerer termiske udsving med spinstrøm(PhysOrg.com) - Et team af forskere fra NIST Center for Nanoscale Science and Technology, universitetet i Münster, og West Virginia University har demonstreret kontrol af magnetiske termiske fluktuati -
 Elektroner på kanten:Atomisk tynde kvantespinhalmaterialerNanyang adjunkt Bent Weber (til venstre) og Dr. Michael S. Lodge i Quantum Spin Hall-laboratoriet. Fotokredit:SPMS Communications, College of Science, NTU Singapore. Quantum spin Hall isolatorer e
Elektroner på kanten:Atomisk tynde kvantespinhalmaterialerNanyang adjunkt Bent Weber (til venstre) og Dr. Michael S. Lodge i Quantum Spin Hall-laboratoriet. Fotokredit:SPMS Communications, College of Science, NTU Singapore. Quantum spin Hall isolatorer e -
 At tage en side fra naturen for at bygge bedre nanomaterialerFig. 1. Græsningsforekomstdiffraktionsdata, der afslører grænsefladestrukturen for alkylthiol Langmuir -monolag (til venstre) og guldnanokrystaller (til højre) samtidigt. (PhysOrg.com) - Nogle gan
At tage en side fra naturen for at bygge bedre nanomaterialerFig. 1. Græsningsforekomstdiffraktionsdata, der afslører grænsefladestrukturen for alkylthiol Langmuir -monolag (til venstre) og guldnanokrystaller (til højre) samtidigt. (PhysOrg.com) - Nogle gan
- Satellit viser, at den tropiske storm Greg bliver påvirket af vindskydning
- Nitten miles op, eksperiment afslører jordmikrobers sandsynlige skæbne på Mars
- Hvordan transit påvirker jobsøgende - den første og sidste kilometer til stationen gør hele fors…
- Alene emissioner fra det globale fødevaresystem truer opvarmning over 1,5°C, men vi kan handle nu …
- Opbygning til super blodmåne formørker finalen
- NASA finder en uorganiseret tropisk storm Arthur nær North Carolinas kyst


