Aftagelig kappe til nanopartikler hjælper dem med at målrette tumorer

Det ydre lag af denne nanopartikel (i gult) falder af i et surt miljø. Billede:Stephen Morton
MIT kemiske ingeniører har designet en ny type nanopartikel til lægemiddellevering, der udnytter en egenskab, der deles af næsten alle tumorer:De er surere end sunde væv.
Sådanne partikler kan målrette mod næsten enhver form for tumor, og kan designes til at bære stort set alle typer lægemidler, siger Paula Hammond, medlem af David H. Koch Institute for Integrative Cancer Research ved MIT og seniorforfatter til et papir, der beskriver partiklerne i tidsskriftet ACS Nano .
Som de fleste andre lægemiddelleverende nanopartikler, de nye MIT-partikler er indhyllet i et polymerlag, der beskytter dem mod at blive nedbrudt af blodbanen. Imidlertid, MIT-teamet, herunder hovedforfatter og postdoktor Zhiyong Poon, designet dette ydre lag til at falde af efter at være kommet ind i det lidt mere sure miljø nær en tumor. Det afslører et andet lag, der er i stand til at trænge ind i individuelle tumorceller.
I den ACS Nano papir, som gik online 23. april, forskerne rapporterede, at hos mus, deres partikler kan overleve i blodbanen i op til 24 timer, akkumuleres på tumorsteder og trænger ind i tumorceller.
Et nyt mål
Den nye MIT-tilgang adskiller sig fra den, der er taget af de fleste nanopartikeldesignere. Typisk, forskere forsøger at målrette deres partikler mod en tumor ved at dekorere dem med molekyler, der binder specifikt til proteiner, der findes på overfladen af kræftceller. Problemet med den strategi er, at det er svært at finde det rigtige mål - et molekyle, der findes på alle kræftcellerne i en bestemt tumor, men ikke på raske celler. Også, et mål, der virker for én type kræft, virker måske ikke for en anden.
Hammond og hendes kolleger besluttede at drage fordel af tumorens surhedsgrad, som er et biprodukt af dets forstærkede stofskifte. Tumorceller vokser og deler sig meget hurtigere end normale celler, og at metabolisk aktivitet bruger meget ilt, hvilket øger surhedsgraden. Efterhånden som tumoren vokser, vævet bliver mere og mere surt.
For at bygge deres målrettede partikler, forskerne brugte en teknik kaldet "lag-for-lag-samling." Det betyder, at hvert lag kan skræddersyes til at udføre en bestemt funktion.
Når det ydre lag (lavet af polyethylenglycol, eller PEG) nedbrydes i tumorens sure miljø, et positivt ladet mellemlag afsløres. Den positive ladning hjælper med at overvinde en anden hindring for levering af nanopartiklers lægemiddel:Når partiklerne når en tumor, det er svært at få dem til at komme ind i cellerne. Partikler med en positiv ladning kan trænge ind i den negativt ladede cellemembran, men sådanne partikler kan ikke injiceres i kroppen uden en "kappe" af en eller anden art, fordi de også ville ødelægge sunde væv.

Polymerbelægningen (lyseblå) afgives, når partiklen nærmer sig en tumor, afsløre positive ladninger. Disse ladninger hjælper partiklen med at blive absorberet gennem tumorcellemembranen. Billede:Stephen Morton
Nanopartiklernes inderste lag kan være en polymer, der bærer et kræftlægemiddel, eller en kvanteprik, der kunne bruges til billeddannelse, eller stort set alt andet, som designeren måtte ønske at levere, siger Hammond, som er Bayer-professor i kemiteknik ved MIT.
Lag for lag
Andre forskere har forsøgt at designe nanopartikler, der udnytter tumorernes surhedsgrad, men Hammonds partikler er de første, der med succes er blevet testet i levende dyr.
Jinming Gao, professor i onkologi og farmakologi ved University of Texas Southwestern Medical Center, siger, at det er "ganske smart" at bruge lag-for-lag-samling til at skabe partikler med et beskyttende lag, der kan udskilles, når partiklerne når deres mål. "Det er et godt proof of concept, ”Siger Gao, som ikke var en del af forskerholdet. "Dette kunne tjene som en generel strategi til at målrette surt tumormikromiljø for forbedret lægemiddellevering."
Forskerne planlægger at videreudvikle disse partikler og teste deres evne til at levere lægemidler til dyr. Hammond siger, at hun forventer, at det kan tage fem til 10 års udvikling, før kliniske forsøg med mennesker kan begynde.
Hammonds team arbejder også på nanopartikler, der kan bære flere nyttelaster. For eksempel, det ydre PEG-lag kan bære et lægemiddel eller et gen, der ville "prime" tumorcellerne til at være modtagelige for et andet lægemiddel, der bæres i partiklens kerne.
Denne historie er genudgivet med tilladelse fra MIT News (web.mit.edu/newsoffice/), et populært websted, der dækker nyheder om MIT-forskning, innovation og undervisning.
Sidste artikelSolvarme-fladpaneler, der genererer elektrisk strøm
Næste artikelAt spille pool med atomer
 Varme artikler
Varme artikler
-
 Hjerteceller på laboratoriechippen viser nanosense, der styrer adfærdJohns Hopkins og koreanske forskere udviklede denne chip til at dyrke hjerteceller, der minder mere om naturligt hjertevæv. Kredit:Will Kirk/JHU Johns Hopkins biomedicinske ingeniører, arbejde med
Hjerteceller på laboratoriechippen viser nanosense, der styrer adfærdJohns Hopkins og koreanske forskere udviklede denne chip til at dyrke hjerteceller, der minder mere om naturligt hjertevæv. Kredit:Will Kirk/JHU Johns Hopkins biomedicinske ingeniører, arbejde med -
 Ny lægemiddelformuleringsmetode kan føre til mindre pillerMIT kemiingeniører har udtænkt en ny måde at formulere hydrofobe lægemidler ved at omdanne dem til en nanoemulsion, som kan hældes i en form og tørres til tabletter. Nanoemulsionen kan også bruges til
Ny lægemiddelformuleringsmetode kan føre til mindre pillerMIT kemiingeniører har udtænkt en ny måde at formulere hydrofobe lægemidler ved at omdanne dem til en nanoemulsion, som kan hældes i en form og tørres til tabletter. Nanoemulsionen kan også bruges til -
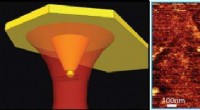 Forskere laver næste generations kemiske kortlægninger på nanoskalaenSkematisk af koaksial sonde til billeddannelse af et carbon nanorør (til venstre) og et kemisk kort over carbon nanorør med kemisk og (højre) topografisk information ved hver pixel. (Billede fra Weber
Forskere laver næste generations kemiske kortlægninger på nanoskalaenSkematisk af koaksial sonde til billeddannelse af et carbon nanorør (til venstre) og et kemisk kort over carbon nanorør med kemisk og (højre) topografisk information ved hver pixel. (Billede fra Weber -
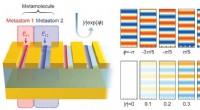 Ny grafenbaseret metasurface, der er i stand til uafhængig amplitude og fasekontrol af lysEt skematisk billede af grafen plasmoniske metamolekyler, der er i stand til uafhængig amplitude og fasekontrol af lys. Kredit:KAIST Forskere beskrev en ny strategi for at designe metamolekyler, d
Ny grafenbaseret metasurface, der er i stand til uafhængig amplitude og fasekontrol af lysEt skematisk billede af grafen plasmoniske metamolekyler, der er i stand til uafhængig amplitude og fasekontrol af lys. Kredit:KAIST Forskere beskrev en ny strategi for at designe metamolekyler, d
- Hvorfor vil nogle forskere sprede rør gennem det åbne hav?
- Hvordan man laver siliciumkrystaller fra Sand
- Minoriteter ramt hårdest af studielånsgæld under recession, undersøgelse finder
- Vil du have, at borgerne bekymrer sig om klimaforandringerne? Skriv en check til dem
- De syv mest ekstreme planeter, der nogensinde er opdaget
- Tilfældighed åbner portene til attophotografiens land


