Nanosensorer lavet af DNA kan lette vejen til nye kræfttests og lægemidler
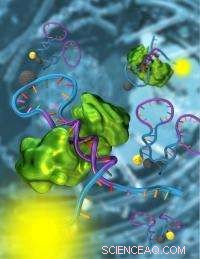
En strukturskiftende nanosensor lavet af DNA (blå og lilla) registrerer en specifik transkriptionsfaktor (grøn). Ved at bruge disse nanosensorer, et team af forskere fra UCSB har demonstreret påvisning af transkriptionsfaktorer direkte i cellulære ekstrakter. Forskerne mener, at deres strategier vil give biologer mulighed for at overvåge aktiviteten af tusindvis af transkriptionsfaktorer, fører til en bedre forståelse af mekanismerne bag celledeling og udvikling. Kredit:Peter Allen
Sensorer lavet af tilpassede DNA-molekyler kan bruges til at tilpasse kræftbehandlinger og overvåge kvaliteten af stamceller, ifølge et internationalt hold af forskere ledet af forskere ved UC Santa Barbara og Universitetet i Rom Tor Vergata.
De nye nanosensorer kan hurtigt detektere en bred klasse af proteiner kaldet transkriptionsfaktorer, som fungerer som livets hovedkontrolkontakter. Forskningen er beskrevet i en artikel publiceret i Journal of the American Chemical Society .
"Vores cellers skæbne styres af tusindvis af forskellige proteiner, kaldet transkriptionsfaktorer, " sagde Alexis Vallée-Bélisle, en postdoktor i UCSB's Institut for Kemi og Biokemi, der ledede undersøgelsen. "Disse proteiners rolle er at læse genomet og omsætte det til instruktioner for syntesen af de forskellige molekyler, der sammensætter og styrer cellen. Transskriptionsfaktorer virker lidt ligesom vores cellers 'indstillinger', ligesom indstillingerne på vores telefoner eller computere. Det, vores sensorer gør, er at læse disse indstillinger."
Når videnskabsmænd tager stamceller og forvandler dem til specialiserede celler, de gør det ved at ændre niveauet af nogle få transkriptionsfaktorer, forklarede han. Denne proces kaldes celle omprogrammering. "Vores sensorer overvåger transkriptionsfaktoraktiviteter, og kunne bruges til at sikre, at stamceller er blevet korrekt omprogrammeret, " sagde Vallée-Bélisle. "De kunne også bruges til at bestemme, hvilke transkriptionsfaktorer der aktiveres eller undertrykkes i en patients kræftceller, dermed gør det muligt for læger at bruge den rigtige kombination af lægemidler til hver patient."
Andrew Bonham, en postdoc ved UCSB og medførsteforfatter af undersøgelsen, forklaret, at mange laboratorier har opfundet måder at læse transkriptionsfaktorer på; imidlertid, dette teams tilgang er meget hurtig og bekvem. "I de fleste laboratorier, forskere bruger timer på at udvinde proteinerne fra celler, før de analyserer dem, " sagde Bonham. "Med de nye sensorer, vi maser bare cellerne sammen, sæt sensorerne i, og mål niveauet af fluorescens af prøven."
Denne internationale forskningsindsats –– organiseret af seniorforfatterne Kevin Plaxco, professor i UCSB's Institut for Kemi og Biokemi, og Francesco Ricci, professor ved universitetet i Rom, Tor Vergata –– startede, da Ricci indså, at al den information, der er nødvendig for at detektere transkriptionsfaktoraktiviteter, allerede er krypteret i det menneskelige genom, og kunne bruges til at bygge sensorer. "Ved aktivering, disse tusindvis af forskellige transkriptionsfaktorer binder til deres egen specifikke mål-DNA-sekvens, " sagde Ricci. "Vi bruger disse sekvenser som udgangspunkt for at bygge vores nye nanosensorer."
Det vigtigste gennembrud bag denne nye teknologi kom fra studier af de naturlige biosensorer inde i celler. "Alle skabninger, fra bakterier til mennesker, overvåge deres omgivelser ved hjælp af 'biomolekylære switches' – formændrende molekyler lavet af RNA eller proteiner, " sagde Plaxco. "F.eks. i vores bihuler, der er millioner af receptorproteiner, der detekterer forskellige lugtmolekyler ved at skifte fra en 'off-tilstand' til en 'on-tilstand'. Skønheden ved disse kontakter er, at de er små nok til at fungere inde i en celle, og specifik nok til at arbejde i de meget komplekse miljøer, der findes der."
Inspireret af effektiviteten af disse naturlige nanosensorer, forskergruppen gik sammen med Norbert Reich, også professor i UCSB's Institut for Kemi og Biokemi, at bygge syntetiske skiftende nanosensorer ved hjælp af DNA, snarere end proteiner eller RNA.
Specifikt, holdet omkonstruerede tre naturligt forekommende DNA-sekvenser, hver genkender en anden transkriptionsfaktor, til molekylære switches, der bliver fluorescerende, når de binder til deres tilsigtede mål. Ved at bruge disse sensorer i nanometerskala, forskerne kunne bestemme transkriptionsfaktoraktivitet direkte i cellulære ekstrakter ved blot at måle deres fluorescensniveau.
Forskerne mener, at denne strategi i sidste ende vil give biologer mulighed for at overvåge aktiveringen af tusindvis af transkriptionsfaktorer, fører til en bedre forståelse af mekanismerne bag celledeling og udvikling. "Alternativt da disse nanosensorer arbejder direkte i biologiske prøver, vi tror også, at de kan bruges til at screene og teste nye lægemidler, der for eksempel, hæmmer transkriptionsfaktorbindingsaktivitet, der er ansvarlig for væksten af tumorceller, " sagde Plaxco.
Sidste artikelMønstret medieteknik opnår Terabit -dataoptagelsestætheder
Næste artikelEn innovativ metode til måling af nanopartikler
 Varme artikler
Varme artikler
-
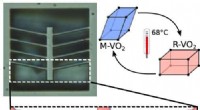 Ny tænd/sluk-funktion for hurtig, følsom, ultra-små teknologierBright-field mikroskopi billede af en VO 2 plan aktuator af chevron-typen. Superposition i falsk farve af spidsen af skytten ved lav og høj temperatur. Bar, 1 μm. Kredit:Osaka University Hvord
Ny tænd/sluk-funktion for hurtig, følsom, ultra-små teknologierBright-field mikroskopi billede af en VO 2 plan aktuator af chevron-typen. Superposition i falsk farve af spidsen af skytten ved lav og høj temperatur. Bar, 1 μm. Kredit:Osaka University Hvord -
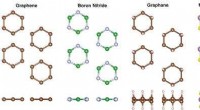 Supercomputere afslører mærkelige, stress-inducerede transformationer i verdens tyndeste materiale…Set ovenfra og fra siden af blød tilstand ustabilitet i anstrengte monolag materialer. I grafen, bornitrid, og grafan rygraden forvrænges mod isolerede seks-atom ringe, mens molybdændisulfid gennemg
Supercomputere afslører mærkelige, stress-inducerede transformationer i verdens tyndeste materiale…Set ovenfra og fra siden af blød tilstand ustabilitet i anstrengte monolag materialer. I grafen, bornitrid, og grafan rygraden forvrænges mod isolerede seks-atom ringe, mens molybdændisulfid gennemg -
 Ingeniører øger produktionen af solafsaltningssystem med 50 %Koncentrering af sollys på bittesmå pletter på den varmegenererende membran udnytter et iboende og hidtil ukendt ikke-lineært forhold mellem fototermisk opvarmning og damptryk. Kredit:Pratiksha Dongar
Ingeniører øger produktionen af solafsaltningssystem med 50 %Koncentrering af sollys på bittesmå pletter på den varmegenererende membran udnytter et iboende og hidtil ukendt ikke-lineært forhold mellem fototermisk opvarmning og damptryk. Kredit:Pratiksha Dongar -
 Nanovidenskab går stort:Opdagelse kan føre til forbedret elektronikJen Cha, en UC San Diego nanoingeniør professor, skubber på hylderne inden for nanovidenskab ved at bruge biologi til at konstruere samlingen af materialer i nanoskala til anvendelser inden for medi
Nanovidenskab går stort:Opdagelse kan føre til forbedret elektronikJen Cha, en UC San Diego nanoingeniør professor, skubber på hylderne inden for nanovidenskab ved at bruge biologi til at konstruere samlingen af materialer i nanoskala til anvendelser inden for medi
- Undersøgelse finder plads til forbedringer i Sydkoreas forurenede vandløb
- Overvågning af aktivitet i det geosynkrone bånd
- Sådan laver du en 3D-model af åndedrætssystemet
- Vand gør ledninger endnu mere nano:Lab udvider meniskmaske-processen til at lave under 10 nanometer…
- Rumsommerfugl er hjemsted for hundredvis af babystjerner
- Hjertelandet er altid et sted med global forbindelse, ikke isolation, siger forfatteren


