Nanopartikler genstarter blodgennemstrømningen i hjernen
En nanopartikel udviklet på Rice University og testet i samarbejde med Baylor College of Medicine (BCM) kan give store fordele til akutbehandlingen af hjerneskadeofre, selv dem med lettere skader.
Kombinerede polyethylenglycol-hydrofile kulstofklynger (PEG-HCC), allerede testet for at forbedre kræftbehandlingen, er også dygtige antioxidanter. I dyreforsøg, injektioner af PEG-HCC under indledende behandling efter en skade hjalp med at genoprette balancen i hjernens vaskulære system.
Resultaterne blev rapporteret i denne måned i tidsskriftet American Chemical Society ACS Nano .
En PEG-HCC-infusion, der hurtigt stabiliserer blodgennemstrømningen i hjernen, ville være et væsentligt fremskridt for nødhjælpsarbejdere og slagmarksmedicinere, sagde Rice kemiker og medforfatter James Tour.
"Dette kan være en første forsvarslinje mod reaktive oxygenarter (ROS), der altid overstimuleres under et medicinsk traume, hvad enten det er til et ulykkesoffer eller en såret soldat, " sagde Tour, Rice's T.T. og W.F. Chao Chair i kemi samt professor i maskinteknik og materialevidenskab og i datalogi. "De forværres bestemt, når der er traumer med massivt blodtab."
Ved en traumatisk hjerneskade, celler frigiver en for stor mængde af en ROS kendt som superoxid (SO) i blodet. Superoxider er giftige frie radikaler, molekyler med en uparret elektron, som immunsystemet normalt bruger til at dræbe invaderende mikroorganismer. Sunde organismer balancerer SO med superoxiddismutase (SOD), et enzym, der neutraliserer det. Men selv milde hjernetraumer kan frigive superoxider på niveauer, der overvælder hjernens naturlige forsvar.
"Superoxid er den mest skadelige af de reaktive oxygenarter, da det er stamfader til mange af de andre, " sagde Tour. "Hvis du ikke beskæftiger dig med SÅ, det danner peroxynitrit og hydrogenperoxid. SO er opstrøms forløber for mange af downstream-problemerne."
SO påvirker den autoregulerende mekanisme, der styrer det følsomme cirkulationssystem i hjernen. Normalt, kar udvides, når blodtrykket er lavt og trækker sig sammen, når det er højt, for at opretholde en ligevægt, men manglende regulering kan føre til hjerneskade ud over, hvad der kan være forårsaget af det indledende traume.
"Der er mange facetter af hjerneskade, der i sidste ende bestemmer, hvor meget skade der vil være, sagde Thomas Kent, avisens medforfatter, en BCM-professor i neurologi og chef for neurologi ved Michael E. DeBakey Veterans Affairs Medical Center i Houston. "Den ene er den første skade, og det er stort set gjort på få minutter. Men en række ting, der sker senere, gør ofte tingene værre, og det er der, vi kan gribe ind."
Kent nævnte som eksempel det andet udbrud af frie radikaler, der kan opstå efter genoplivning efter skade. "Det er det, vi kan behandle:den yderligere skade, der sker på grund af nødvendigheden af at genoprette nogens blodtryk, som giver ilt, der fører til flere skadelige frie radikaler."
I test, forskerne fandt, at PEG-HCC nanopartikler øjeblikkeligt og fuldstændigt slukkede superoxidaktivitet og gjorde det muligt for det autoregulatoriske system hurtigt at genvinde balancen. Tour sagde, at ROS-molekyler let kombineres med PEG-HCC'er, genererer "en uskadelig carbon dobbeltbinding, så det er virkelig en radikal udslettelse. Der er ingen sådan mekanisme i biologi." Mens et SOD-enzym kun kan ændre ét superoxidmolekyle ad gangen, et enkelt PEG-HCC på størrelse med et stort protein på 2-3 nanometer bredt og 30-40 nanometer langt kan slukke hundreder eller tusinder. "Dette er en lejlighed, hvor en pakke i nanostørrelse gør noget, som intet lille lægemiddel eller protein kunne gøre, understreger effektiviteten af aktive nano-baserede lægemidler."
"Dette er det mest bemærkelsesværdigt effektive, jeg nogensinde har set, " sagde Kent. "Bogstaveligt talt inden for få minutter efter at have injiceret det, cerebral blodgennemstrømning er tilbage til normal, og vi kan holde det der med blot en simpel anden indsprøjtning. Til sidst, vi har normaliseret de frie radikaler og samtidig bevaret nitrogenoxid (som er afgørende for autoregulering). Disse partikler viste den antioxidantmekanisme, vi tidligere havde identificeret som forudsigende for effektivitet."
De første spor til PEG-HCC's antioxidantevne kom under toksicitetsundersøgelser af nanopartikler med MD Anderson Cancer Center. "Vi bemærkede, at de sænkede alkalisk fosfatase i leveren, " sagde Tour. "En af vores Baylor-kolleger så dette og sagde, 'Hej, det ser ud til, at det faktisk får levercellerne til at leve længere end normalt.'
"Oxidativ ødelæggelse af leverceller er normal, så det fik os til at tro, at disse kunne være rigtig gode radikale skure, " sagde Tour.
Kent sagde, at nanopartiklerne som testet ikke viste tegn på toksicitet, men eventuelle resterende bekymringer bør besvares med yderligere test. Forskerne fandt, at halveringstiden for PEG-HCC'er i blodet - den tid, det tager for halvdelen af partiklerne at forlade kroppen - er mellem to og tre timer. Tests med forskellige celletyper in vitro viste ingen toksicitet, han sagde.
Forskningen har også implikationer for slagtilfældeofre og organtransplanterede patienter, sagde Tour.
Næste, holdet håber at få et andet laboratorium til at gentage dets positive resultater. "Vi har gentaget det nu tre gange, og vi fik de samme resultater, så vi er sikre på, at det fungerer i vores hænder, " sagde Kent.
 Varme artikler
Varme artikler
-
 Nanovidenskab går stort:Opdagelse kan føre til forbedret elektronikJen Cha, en UC San Diego nanoingeniør professor, skubber på hylderne inden for nanovidenskab ved at bruge biologi til at konstruere samlingen af materialer i nanoskala til anvendelser inden for medi
Nanovidenskab går stort:Opdagelse kan føre til forbedret elektronikJen Cha, en UC San Diego nanoingeniør professor, skubber på hylderne inden for nanovidenskab ved at bruge biologi til at konstruere samlingen af materialer i nanoskala til anvendelser inden for medi -
 Hurtigere, billigere DNA-sekventeringsmetode udvikletEt team af forskere ledet af Boston Universitys biomedicinske ingeniør Amit Meller bruger elektriske felter til effektivt at tegne lange DNA-strenge gennem nanopore-sensorer, drastisk reduktion af ant
Hurtigere, billigere DNA-sekventeringsmetode udvikletEt team af forskere ledet af Boston Universitys biomedicinske ingeniør Amit Meller bruger elektriske felter til effektivt at tegne lange DNA-strenge gennem nanopore-sensorer, drastisk reduktion af ant -
 Enheden måler fordelingen af små partikler, når de strømmer gennem en mikrofluidisk kanalEn suspenderet mikrokanalresonator (SMR) måler partiklernes masser, når de strømmer gennem en smal kanal. Den originale massesensor består af en væskefyldt mikrokanal ætset i en lille siliciumudkrager
Enheden måler fordelingen af små partikler, når de strømmer gennem en mikrofluidisk kanalEn suspenderet mikrokanalresonator (SMR) måler partiklernes masser, når de strømmer gennem en smal kanal. Den originale massesensor består af en væskefyldt mikrokanal ætset i en lille siliciumudkrager -
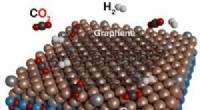 Producerer grafen fra kuldioxidKuldioxid (rød-sort) og hydrogen (grå) reagerer katalytisk på grafen (sort) på kobber-palladiumoverflader. Kredit:E. Moreno-Pineda, KIT Den brede offentlighed kender den kemiske forbindelse af kul
Producerer grafen fra kuldioxidKuldioxid (rød-sort) og hydrogen (grå) reagerer katalytisk på grafen (sort) på kobber-palladiumoverflader. Kredit:E. Moreno-Pineda, KIT Den brede offentlighed kender den kemiske forbindelse af kul
- InSight fanger stråler på Mars
- NASA fanger overgangen fra den tropiske storm Francisco nær den koreanske halvø
- Brug af fiberoptiske kabler til at detektere jordskælv
- Spædbørn har mere mikroplastik i deres afføring end voksne, undersøgelse finder
- Zapping af jorden med elektricitet for at skabe detaljerede jordbundskort til gårde
- Diffusion: Hvad er det? & Hvordan sker det?


