I verdens første, atomkraftmikroskop ser kemiske bindinger i individuelle molekyler (m/ video)

Et nanografenmolekyle, der udviser carbon-carbon-bindinger af forskellig længde og bindingsrækkefølge afbildet ved ikke-kontakt atomkraftmikroskopi ved hjælp af en carbonmonoxidfunktionaliseret spids. Dette molekyle blev syntetiseret ved Centre National de la Recherche Scientifique (CNRS) i Toulouse. Kredit:IBM
(Phys.org) – IBM-forskere har været i stand til at differentiere de kemiske bindinger i individuelle molekyler for første gang ved hjælp af en teknik kendt som noncontact atomic force microscopy (AFM).
Resultaterne skubber til udforskningen af at bruge molekyler og atomer i den mindste skala og kan være vigtige for at studere grafenanordninger, som i øjeblikket udforskes af både industrien og den akademiske verden for applikationer, herunder trådløs kommunikation med høj båndbredde og elektroniske skærme.
"Vi fandt to forskellige kontrastmekanismer til at skelne mellem bindinger. Den første er baseret på små forskelle i kraften målt over bindingerne. Vi forventede denne form for kontrast, men det var en udfordring at løse, " sagde IBM-forsker Leo Gross. "Den anden kontrastmekanisme kom virkelig som en overraskelse:Obligationer dukkede op med forskellige længder i AFM-målinger. Ved hjælp af ab initio-beregninger fandt vi ud af, at vipningen af kuliltemolekylet ved spidsens spids er årsagen til denne kontrast."
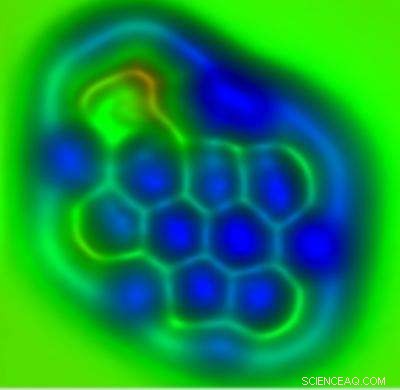
Dette er et nanografenmolekyle, der udviser carbon-carbon-bindinger af forskellig længde og bindingsrækkefølge afbildet ved ikke-kontakt atomkraftmikroskopi ved hjælp af en carbonmonoxidfunktionaliseret spids. Dette molekyle blev syntetiseret af Centro de Investigación en Química Biolóxica e Materiais Moleculares (CIQUS) ved Universidade de Santiago de Compostela. Kredit:IBM
Som rapporteret i forsiden af 14. september-udgaven af Videnskab magasin, IBM Research-forskere afbildede bindingsrækkefølgen og længden af individuelle kulstofbindinger i C 60 , også kendt som en buckyball for sin fodboldform og to plane polycykliske aromatiske kulbrinter (PAH'er), som ligner små flager af grafen. PAH'erne blev syntetiseret af Centro de Investigación en Química Biolóxica e Materiais Moleculares (CIQUS) ved Universidade de Santiago de Compostela og Centre National de la Recherche Scientifique (CNRS) i Toulouse.
De individuelle bindinger mellem kulstofatomer i sådanne molekyler adskiller sig subtilt i deres længde og styrke. Alt det vigtige kemikalie, elektronisk, og optiske egenskaber af sådanne molekyler er relateret til forskellene i bindinger i de polyaromatiske systemer. Nu, for første gang, disse forskelle blev påvist for både individuelle molekyler og bindinger. Dette kan øge den grundlæggende forståelse på niveauet af individuelle molekyler, vigtig for forskning i nye elektroniske enheder, organiske solceller, og organiske lysdioder (OLED'er). I særdeleshed, lempelsen af bindinger omkring defekter i grafen samt ændring af bindinger i kemiske reaktioner og i exciterede tilstande kunne potentielt studeres.
Som i deres tidligere forskning " Den kemiske struktur af et molekyle opløst ved atomkraftmikroskopi " IBM-forskerne brugte et atomic force microscope (AFM) med en spids, der afsluttes med et enkelt carbonmonoxid (CO) molekyle. Denne spids svinger med en lille amplitude over prøven for at måle kræfterne mellem spidsen og prøven, såsom et molekyle, at skabe et billede. CO-termineringen af spidsen fungerer som et kraftigt forstørrelsesglas til at afsløre molekylets atomare struktur, inklusive dets obligationer. Dette gjorde det muligt at skelne individuelle bindinger, der kun adskiller sig med 3 picometer eller 3 × 10- 12 m, som er omkring en hundrededel af et atoms diameter.
I tidligere forskning lykkedes det for holdet at afbilde den kemiske struktur af et molekyle, men ikke de subtile forskelle i bindingerne. Diskriminerende bindingsrækkefølge er tæt på teknikkens nuværende opløsningsgrænse, og ofte slører andre effekter kontrasten relateret til bindingsrækkefølgen. Derfor måtte forskerne udvælge og syntetisere molekyler, hvor forstyrrende baggrundseffekter kunne udelukkes.
To corroborate the experimental findings and gain further insight into the exact nature of the contrast mechanisms, the team performed first-principles density functional theory calculations. Thereby they calculated the tilting of the CO molecule at the tip apex that occurs during imaging. They found how this tilting yields a magnification and the very sharp images of the bonds.
 Varme artikler
Varme artikler
-
 AI finder 2D-materialer på et øjeblikForskere fra University of Tokyo udvikler en maskinlæringsalgoritme til at detektere atomisk tynde 2D-materialer, inklusive grafen, fra et mikroskopbillede på en brøkdel af et sekund - hvilket kan acc
AI finder 2D-materialer på et øjeblikForskere fra University of Tokyo udvikler en maskinlæringsalgoritme til at detektere atomisk tynde 2D-materialer, inklusive grafen, fra et mikroskopbillede på en brøkdel af et sekund - hvilket kan acc -
 Nanotermometer måler temperaturen inde i cellerneRice University kemikere modificerede BODIPY-molekyler til at fungere som nano-termometre inde i celler. Diagrammet til venstre er en samling af fluorescerende levetidsmikrografier, der viser molekyle
Nanotermometer måler temperaturen inde i cellerneRice University kemikere modificerede BODIPY-molekyler til at fungere som nano-termometre inde i celler. Diagrammet til venstre er en samling af fluorescerende levetidsmikrografier, der viser molekyle -
 Forskere leder selvsamlingen af guldnanopartikler til tynde film, der er klar til enhedenBerkeley Lab-forskere har udviklet en relativt enkel og billig teknik til at dirigere selvsamling af nanopartikler til tynde film, der er klar til apparater med mikrodomæner af lamellære (venstre) ell
Forskere leder selvsamlingen af guldnanopartikler til tynde film, der er klar til enhedenBerkeley Lab-forskere har udviklet en relativt enkel og billig teknik til at dirigere selvsamling af nanopartikler til tynde film, der er klar til apparater med mikrodomæner af lamellære (venstre) ell -
 Ultrahurtig laserpuls skabt af gyldne nanopartiklerKredit:Aalto Universitet En ny undersøgelse viser, at organisk farvestof kombineret med metalliske nanostrukturer kan give ultrahurtig laserdynamik med korte og hurtigt optrædende laserimpulser.
Ultrahurtig laserpuls skabt af gyldne nanopartiklerKredit:Aalto Universitet En ny undersøgelse viser, at organisk farvestof kombineret med metalliske nanostrukturer kan give ultrahurtig laserdynamik med korte og hurtigt optrædende laserimpulser.
- Hvordan de blomster, du køber til din mor til Mors Dag, kan være knyttet til den amerikanske krig …
- Hjælper mikrochipindustrien med at gå (meget lavt) med strømmen
- NASA leverer hardware til ESA dark energy-mission
- Organeller findes i både plante og bakterieceller
- Fysikere satte en ny rekord for kvantehukommelses effektivitet
- Sådan løses kubiske ligninger


