Selvmonterende nanofilamenter forbedrer lægemiddeltilførslen
(Phys.org) - Mens de fleste nanopartikler under udvikling som lægemiddelleveringskøretøjer er kugler, en voksende mængde forskning tyder på, at cylindriske nanopartikler ville klare sig endnu bedre ved det dobbelte mål om at overleve i blodstrømmen længe nok til at nå deres tilsigtede mål og trænge ind i cellevæggen for at levere deres terapeutiske nyttelast inde i tumorceller, hvor det er mest nødvendigt. Et team af efterforskere ved Northwestern University Center for Cancer Nanotechnology Excellence (Northwestern CCNE) har opfundet en cylindrisk nanofilamentstruktur, der reducerer tumorvækst betydeligt i en dyremodel af brystkræft.
Et team ledet af Vincent Cryns, der for nylig flyttede fra Northwestern til University of Wisconsin School of Medicine and Public Health, og Samuel Stupp, udviklet de selvsamlende nanofibre. Efterforskerne rapporterer deres fund i journalen ACS Nano .
For at skabe deres tumorhæmmende cylindre, efterforskerne henvendte sig til en familie af molekyler kendt som peptidamfifiler. Når det sættes i vand, disse molekyler, som kan fremstilles ved hjælp af automatiserede peptidsyntesere, som spontant selvsamler sig til lange, tynde filamenter. Afhængigt af valget af udgangsmaterialer, disse filamenter kan vise et stort antal biologisk aktive peptider på deres overflader, der gør det muligt for fibrene at fungere som både lægemidler og lægemiddelafgivende midler samtidigt uden behov for yderligere indkapsling af kræftmidler inden for nanostrukturen.
I tidligere arbejde, det nordvestlige CCNE-team havde vist, at en sådan nanofiber var mere giftig for kræftceller end ikke-maligne celler, men denne nanofiber blev hurtigt nedbrudt i blodstrømmen. For at forbedre de nanofiberers farmakokinetiske egenskaber, efterforskerne oprettede et andet peptidamfifil, denne er knyttet til poly (ethylenglycol) (PEG), en polymer, der i vid udstrækning bruges til at øge overlevelse af nanopartikler i blodstrømmen. Da forskerne blandede peptidamfifilen med den PEGylerede amfifil, de to molekyler samler sig selv i nanofilamenter. Ved at tilføje det PEGylerede peptidamfifil til blandingen øgede forskerne otte gange mængden af intakt nanofiber, der overlevede nedbrydning af enzymet trypsin sammenlignet med den oprindelige nanofiber.
For at se, om denne nanofiber viste løfte i et dyreforsøg, efterforskerne administrerede det til mus med humane brysttumorer. Efter dosering af dyrene to gange ugentligt i tre uger, forskerne observerede, at tumorer i de behandlede dyr voksede meget langsommere end hos kontroldyr. De bemærkede også, at dyrene ikke viste tegn på narkotikarelaterede toksiciteter.
 Varme artikler
Varme artikler
-
 NRI skal lede en ny femårig indsats for at udvikle post-CMOS elektronikEn nanoelektronisk tilgang, der er studeret af NRI MIND-centret, er nanomagnetlogik (NML) - logiske kredsløb, der fungerer ved magnetisk kobling mellem tilstødende nanoskalamagneter. Her, SEM (l) og m
NRI skal lede en ny femårig indsats for at udvikle post-CMOS elektronikEn nanoelektronisk tilgang, der er studeret af NRI MIND-centret, er nanomagnetlogik (NML) - logiske kredsløb, der fungerer ved magnetisk kobling mellem tilstødende nanoskalamagneter. Her, SEM (l) og m -
 Nanokamera tager billeder på afstande, der er mindre end lysets egen bølgelængdeEt billede af Illinois Block I-logoet optaget af plasmonisk film. Hver streg i bogstavet er cirka 6 mikrometer. Kredit:Toussaint Research Group Forskere ved University of Illinois i Urbana-Champai
Nanokamera tager billeder på afstande, der er mindre end lysets egen bølgelængdeEt billede af Illinois Block I-logoet optaget af plasmonisk film. Hver streg i bogstavet er cirka 6 mikrometer. Kredit:Toussaint Research Group Forskere ved University of Illinois i Urbana-Champai -
 Ny mikrobølgebilledfremgangsmåde åbner en nanoskalavisning af processer i væskerNIST- og ORNL-forskere har udtænkt en nærfeltsmikrobølgebilledmetode til at tage billeder af nanoskalaprocesser under naturlige forhold. Når spidsen af et atomkraftmikroskop scanner over en ultratyn
Ny mikrobølgebilledfremgangsmåde åbner en nanoskalavisning af processer i væskerNIST- og ORNL-forskere har udtænkt en nærfeltsmikrobølgebilledmetode til at tage billeder af nanoskalaprocesser under naturlige forhold. Når spidsen af et atomkraftmikroskop scanner over en ultratyn -
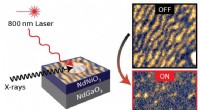 Styring af nikkelat nano-switche med lysSender en meget hurtig, højenergipuls af laserlys hævede temperaturen på en prøve af neodymnikkelat fra 150 til 152 Kelvin i et kort øjeblik. Denne lille temperaturstigning var nok til at ændre materi
Styring af nikkelat nano-switche med lysSender en meget hurtig, højenergipuls af laserlys hævede temperaturen på en prøve af neodymnikkelat fra 150 til 152 Kelvin i et kort øjeblik. Denne lille temperaturstigning var nok til at ændre materi
- USA lancerer med succes en ubemandet genanvendelig drone til rumeksperimenter
- Sådan gør du eksponenter på TI-30XIIS
- NASA ser udviklingen af den tropiske storm Gilma
- Tre måder at smelte en Rock
- New York sigter mod skyskrabere skyhøjt energiforbrug
- En brugervenlig tilgang til aktiv belønningslæring i robotter


