Forskere studerer, hvordan man kan omdanne kræftmedicin til deres egne leveringssystemer
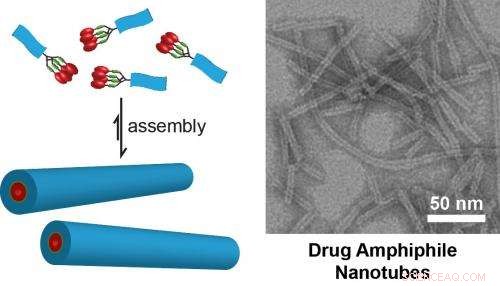
(Venstre) Skematisk illustration af designkonceptet til selvsamlende lægemiddelamfifiler. Lægemiddelbelastningen i de selvsamlede nanostrukturer er defineret af arten af molekylært design. (Til højre) TEM-billede af nanorør dannet ved selvsamling af en lægemiddelamfifil indeholdende fire camptothecin-lægemidler. Disse nanorør har en fast lægemiddelbelastning på 38 % (vægt/vægt). Billede fra Cui Lab ved Johns Hopkins University. Kredit:Cui Lab, Kemisk og biomolekylær ingeniørafdeling, Johns Hopkins University
(Phys.org) — I de seneste år, mange populære kræftbehandlinger har brugt nano, det er, små partikler af polymerer eller kulstofbaserede materialer til at transportere kemoterapimedicin til tumorer på en måde, der specifikt er rettet mod kræftceller, mens man skåner normale celler. Men denne tilgang har flere problemer.
Blandt andet, det er svært at kontrollere mængden af lægemiddel, der er fyldt i bæreren, og, faktisk, alt for ofte er der meget mere "bærer" materiale end lægemiddel. Som resultat, lægemiddelmængden varierer ofte fra partikel til partikel, hvilket betyder, at den afgivne kemoterapidosis kan være inkonsekvent eller ujævn. Også, det syntetiske materiale, der omslutter og afgiver lægemidlet, kan i sig selv være giftigt, forårsager uønskede bivirkninger.
Det ideelle scenarie ville være at finde en måde at omdanne kræftmedicin til deres egne leveringssystemer, og eliminere de syntetiske køretøjer helt.
Honggang Cui, assisterende professor i kemisk og biomolekylær teknik ved Johns Hopkins University forsøger at gøre netop det ved at transformere lægemiddelmolekylerne på en måde, der gør dem i stand til at blive deres egne bærere, en proces kendt som selvmontering.
"Vi ønsker at bruge anti-cancer-lægemidlet til at lave nanopartikler ud af sig selv, " siger Cui, også et tilknyttet fakultetsmedlem af Johns Hopkins Institute for NanoBioTechnology. "Udfordringen er:Hvordan gør vi det?"
Den National Science Foundation (NSF)-finansierede videnskabsmand og hans forskerhold bruger nye molekylære ingeniørteknikker, som de håber vil få lægemiddelmolekylerne til at organisere sig i diskrete og isolerede nanostrukturer, snarere end at forblive i deres nuværende "bulk" form.
Hvis han har succes, arbejdet kunne potentielt forbedre cancerkemoterapi ved at øge behandlingens effektivitet, og reducere dets negative bivirkninger.
I øjeblikket, "i en partikel kan du have 2 procent stofladning, og i en anden, måske 10 procent, og i en anden, ikke noget, slet ingen medicin, " siger han. At lade stofferne transportere sig selv "vil hjælpe det kliniske resultat, Cui tilføjer. "Du får hverken for meget eller for lidt af et stof. Du får den rigtige dosis."
For at omdanne disse lægemidler til deres egne leveringssystemer i nanoskala, de skal blive amfifile, hvilket betyder, at de skal have egenskaber, der både kan lide og ikke kan lide vand.
"Det segment, der ikke kan lide vand, vil drive molekylerne til at samles og danne en molekylær klynge, eller en nanostruktur, på en måde at minimere deres kontakt med vandmolekyler, mens det vandlignende segment vil holde nanostrukturen opløselig i vandig opløsning og forhindre dem i at vokse til større objekter, Cui forklarer.
Få lægemidler har denne dobbelthed, når det kommer til vand. "De fleste er meget hydrofobe; de har dårlig vandopløselighed, " han siger.
At lave vandhadende stoffer, der også kan elske vand, forskerne eksperimenterer med vandopløselige peptider, som er forbindelser, der består af to eller flere aminosyrer, forsøger at inkorporere dem i lægemidlerne via bionedbrydelige linkere, det er, kemiske bindinger, der fungerer som en bro mellem det vandelskende peptid og det vandhadende stof.
Når det virker, "lægemidlet kan blive selvsamlende, " siger han. "Når stoffet får evnen til at samle sig selv, vi vil lege med peptidsekvensen for at få kontrol over dens størrelse, form og overfladekemi.
"Peptidet tilføjer ikke kun det vandelskende segment til selvsamling, men også nye funktioner, der muliggør effektiv regulering af deres samling i forskellige størrelser og former, " tilføjer han. "De kunne være bioaktive, og præsentere signaler for specifik tumormålretning."
Håbet er at producere lægemidler mod kræft, der er supramolekylære nanostrukturer, eller partikler, der består af mere end ét molekyle, som "har høj medicinbelastning og fast stofbelastning, " siger Cui.
"Belastningen i nanostrukturen er defineret af det molekylære design, " tilføjer han "Hvis lægemiddelfraktionen i det designede molekyle er 10 procent, nanostrukturen vil også have 10 procent lægemiddelbelastning. Derfor, gennem molekylært design, man kan præcist indstille lægemiddelbelastningen i nanostrukturen."
Cui udfører sin forskning under en NSF Faculty Early Career Development (CAREER)-pris, der begynder i år. Prisen støtter junior fakulteter, der eksemplificerer rollen som lærer-lærde gennem fremragende forskning, fremragende uddannelse og integration af uddannelse og forskning inden for rammerne af deres organisations mission. NSF finansierer hans arbejde med omkring $500, 000 over fem år.
Cui og hans team offentliggjorde for nylig resultater af deres arbejde i Journal of the American Chemical Society demonstrere princippet om at konstruere selvafgivende supramolekylære anticancerlægemidler. Deres arbejde producerede nanofibre og nanorør dannet ved selvsamling af peptid-anticancer-konjugater.
Som en del af bevillingens uddannelsesopsøgende arbejde, Cui planlægger at invitere lokale gymnasie- og mellemskoleelever til at tilbringe tid i sit laboratorium.
"Narkotikalevering er i sagens natur et tværfagligt område, der tilbyder enorme muligheder for uddannelse på alle niveauer, " siger han. "Vi ønsker især at engagere den indre bys offentlige skoleelever til at lære om systemer til levering af stoffer, og de bedste måder at forbedre kræftbehandlingen på."
Mens hans ideer stadig er langt fra klinisk brug, Cui mener, at det i sidste ende vil være muligt at omdanne lægemidler til molekylære byggesten, der vil fungere som deres egne leveringssystemer.
"Jeg kan ikke se nogen grunde til, at disse selvudleverende lægemidler ikke kan oversættes til kliniske omgivelser, når vi først finder ud af måder at manipulere deres selvsamlende adfærd på, " han siger.
 Varme artikler
Varme artikler
-
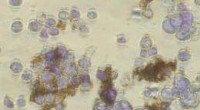 Magnetiske nanopartikler viser løfte om at bekæmpe kræft hos menneskerNanopartikler, i brun, binder sig til kræftceller, i violet, fra menneskets bughule. Kredit:Ken Scarberry/Georgia Tech Forskere ved Georgia Tech og Ovarian Cancer Institute har videreudviklet en p
Magnetiske nanopartikler viser løfte om at bekæmpe kræft hos menneskerNanopartikler, i brun, binder sig til kræftceller, i violet, fra menneskets bughule. Kredit:Ken Scarberry/Georgia Tech Forskere ved Georgia Tech og Ovarian Cancer Institute har videreudviklet en p -
 Farver på sommerfuglevinger giver spor til lysændrende strukturerDen levende grønne farve på skæl af denne Papilionid sommerfugl er produceret af optisk effektive enkelt gyroide fotoniske krystaller. (PhysOrg.com) -- I hjertet af nogle af de mest strålende farv
Farver på sommerfuglevinger giver spor til lysændrende strukturerDen levende grønne farve på skæl af denne Papilionid sommerfugl er produceret af optisk effektive enkelt gyroide fotoniske krystaller. (PhysOrg.com) -- I hjertet af nogle af de mest strålende farv -
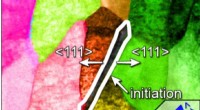 Modarbejde korrosion af olie-rørledning ved at identificere en nanoskala-skurkEt Sandia National Laboratories transmissionselektronmikroskop hjalp med at skabe dette fase -ligevægtskort, der viser områder, hvor korrosion af stål blev observeret ved det tredobbelte kryds, der da
Modarbejde korrosion af olie-rørledning ved at identificere en nanoskala-skurkEt Sandia National Laboratories transmissionselektronmikroskop hjalp med at skabe dette fase -ligevægtskort, der viser områder, hvor korrosion af stål blev observeret ved det tredobbelte kryds, der da -
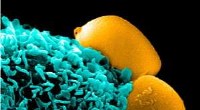 Nanopartikler, der ser ud, fungere som cellerCamouflerede nanopartikler (gule) skjult i membranerne af hvide blodlegemer hviler på overfladen af en immunsystemcelle (fagocyt, blå) uden at blive genkendt, indtaget, og ødelagt (Phys.org) – V
Nanopartikler, der ser ud, fungere som cellerCamouflerede nanopartikler (gule) skjult i membranerne af hvide blodlegemer hviler på overfladen af en immunsystemcelle (fagocyt, blå) uden at blive genkendt, indtaget, og ødelagt (Phys.org) – V
- Tager ansvaret:Forskere går sammen om at lave bedre batterier
- Jeg er en tumor, og jeg er herovre! Nanovaults plejede at stimulere immunsystemet til at bekæmpe kr…
- Hvad betyder en hygrometermåling?
- Hvordan virker lithium-ion-batterier?
- Undersøgelse finder potentiel ustabilitet i Atlanterhavets vandcirkulationssystem
- Sådan finder du terningroot i Ti-84


